Введение
Транзиторная дозозависимая анемия является известным последствием терапии руксолитинибом, оказывающим влияние на тактику относительно старта, режима дозирования и прекращения терапии. При этом влияние новой или прогрессирующей анемии на фоне приема руксолитиниба на эффективность препарата недостаточно изучено. Недавний анализ объединенных данных исследований COMFORT-I/II продемонстрировал, что новая или прогрессирующая анемия не влияет на клинические исходы, такие как уменьшение объема селезенки или контроль симптомов.2
С целью подтверждения этого результата был проведен анализ данных исследования JUMP — крупнейшего исследования по применению руксолитиниба у пациентов с миелофиброзом (МФ).1
Методы
Исследование JUMP представляет собой крупное (N=2233) одногрупповое исследование 3b фазы с расширенным доступом, в котором пациенты с МФ получали терапию руксолитинибом в условиях, аналогичных рутинной клинической практике. Проводилась оценка безопасности и эффективности руксолитиниба у пациентов в возрасте ≥18 лет с диагностированным первичным или вторичным МФ промежуточного риска (Int-1, Int-2) или высокого риска (критерии международной прогностической системы оценки, IPSS) с исходным уровнем тромбоцитов ≥50×109/Л. Все пациенты получали руксолитиниб два раза в сутки в начальной дозировке 5–20 мг с учетом исходного уровня тромбоцитов. В этом апостериорном анализе пациенты изначально были стратифицированы на основании данных по анемии, вызванной МФ (анемия определялась как уровень гемоглобина [Hb] <100 г/Л), и статуса переливания крови у пациентов с анемией (требующая гемотрансфузии анемия [ТГА, получено ≥2 единиц эритроцитов за 8 недель до первой дозы руксолитиниба] или не требующая гемотрансфузии анемия [НТГА]). Результаты были стратифицированы по наличию или отсутствию новой или прогрессирующей анемии после начала приема руксолитиниба (определяемой как снижение уровня гемоглобина на ≥15 г/л или необходимость нового переливания крови на 4, 8 или 12 неделе). Оцениваемые результаты включали ответ со стороны селезенки (определяемый как уменьшение ≥50% на 24 или 48 неделе от исходного уровня, пальпаторно), увеличение ≥6,5 баллов по функциональной шкале общего балла терапии рака и лимфомы (FACT-Lym TS) от исходного уровня на 24-й и 48-й неделе и общую выживаемость (ОВ), измеряемую по методу Каплана-Майера.
Результаты
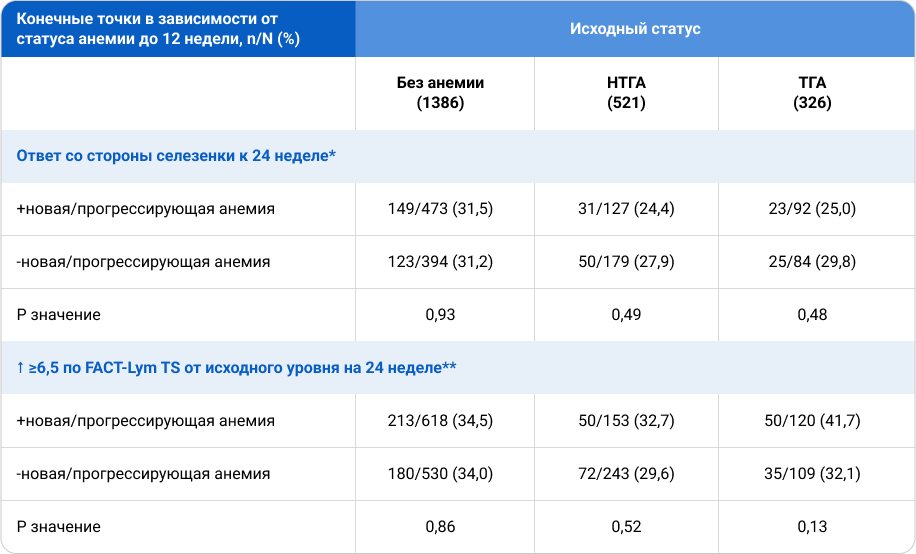
В анализ были включены данные 2233 пациентов (исходный статус: отсутствие анемии, n=1386 [62,1%]; НТГА, n=521 [23,3]; TГА, n=326 [14,6]). Медиана (диапазон) возраста всех пациентов составила 67,0 (18–89) лет; 54,5% пациентов составляли мужчины. Исходные характеристики были сопоставимы между пациентами с или без новой/прогрессирующей анемии. Частота ответа со стороны селезенки на 24-й неделе среди пациентов с новой или прогрессирующей анемией по сравнению с пациентами без нее составила 31,5% vs 31,2%, соответственно (у пациентов без анемии; P=0,93), 24,4% vs 27,9% (НТГА; P=0,49) и 25,0% vs 29,8. % (ТГА; P=0,48) (Таблица 1). Ответ FACT-Lym TS на 24 неделе для пациентов с новой/прогрессирующей анемией по сравнению с пациентами без нее составил 34,5% vs 34,0% (без анемии; P=0,86), 32,7% vs 29,6% (НТГА; P=0,52) и 41,7% vs 32,1%. (ТГА; P=0,13). Подобные же тенденции наблюдались на 48-й неделе среди пациентов с наличием и без новой/прогрессирующей анемии как для показателя ответа со стороны селезенки (35,6% vs 26,1%; P=0,02 [без анемии], 29,6% vs 27,2%; P=0,71 [НТГА] и 19,0% vs 33,3%; P=0,10 [ТГА]) , так и для показателя FACT-Lym (30,4% vs 23,3%; P=0,02 [без анемии], 26,4% vs 27,6%; P=0,84 [НТГА] и 34,2% vs 33,3%; P= 0,91 [ТГА]).
Таблица 1. Результаты анализа исследования JUMP, стратифицированные по исходному статусу анемии и гемотрансфузии, а также по регистрации новой/прогрессирующей анемии.
*полный набор анализов; ** оцениваемая популяция, n=1773
FACT-Lym TS — Functional Assessment of Cancer Therapy — Lymphoma; n/N — число пациентов достигших конечной точки/число подлежащих оценке пациентов (как в категории с исходной анемией и гемотрансфузионном статусе, так и в категории с анемией до 12 недели); НТГА — анемия, не требующая гемотрансфузии; ТГА — анемия, требующая гемотрансфузии; ответ со стороны селезенки — уменьшение размеров селезенки ≥50% от исходного уровня.
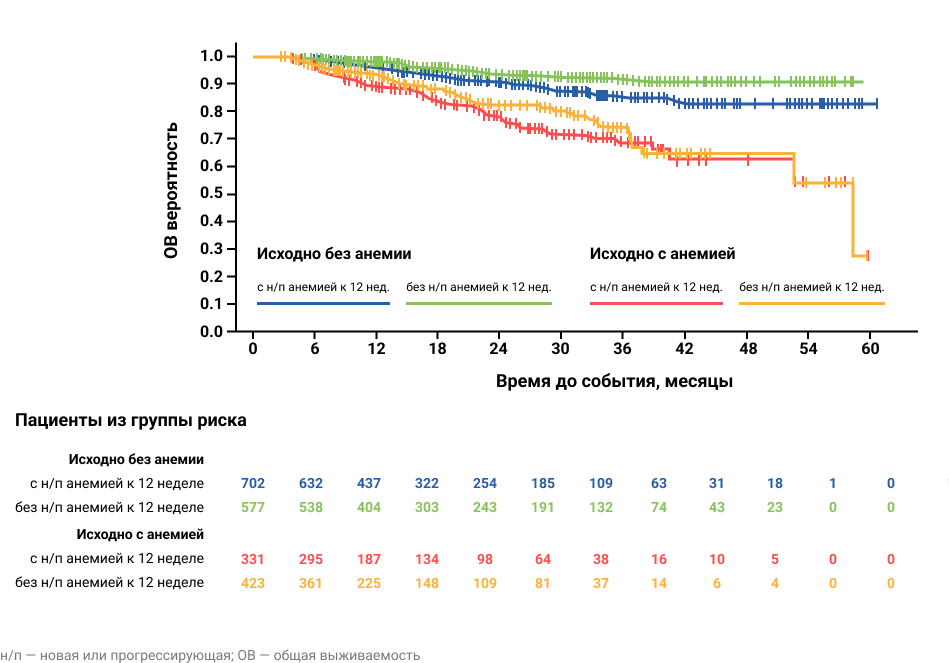
Для пациентов без анемии на исходном уровне время достижения медианы ОВ не было достигнуто ни в одной когорте; однако отмечен лучший показатель ОВ у пациентов без анемии по сравнению с пациентами с зафиксированной новой/прогрессирующей анемией (отношение рисков: 0,559, [95% ДИ: 0,357–0,876]; P=0,01) (Рис.1). Для пациентов с исходной анемией (НТГА и ТГА) не наблюдалось различий в ОВ при наличии или без новой/прогрессирующей анемии (P=0,24).
Рисунок 1. Общая выживаемость у пациентов в исследовании JUMP.
Заключение
Анализ данных исследования JUMP демонстрирует, что выявление новой или прогрессирующей анемии на фоне лечения руксолитинибом не уменьшает клиническую пользу от терапии препаратом. Терапия руксолитинибом была ассоциирована с улучшением таких показателей как размер селезенки и выраженность симптомов заболевания независимо от исходной анемии и статуса переливания крови. Эти результаты согласуются с недавним анализом объединенных данных исследований COMFORT-I/II (n=277), в котором сообщалось об аналогичных результатах в отношении объема селезенки и выраженности симптомов. В отличие от контролируемых клинических исследований COMFORT-I/II, исследование JUMP отражает реальную практику и охватывает более широкую популяцию пациентов с МФ, включая пациентов с количеством тромбоцитов <100×109/Л и МФ низкого риска. В совокупности эти результаты поддерживают применение руксолитиниба в реальной клинической практике у пациентов с МФ независимо от наличия исходной анемии или развития анемии, связанной с лечением.
Список литературы
- Vikas Gupta, Paola Guglielmelli, JE Hamer-Maansson, Evan M. Braunstein, Haifa Kathrin Al-Ali. Effect of New or Worsening Anemia on Clinical Outcomes in 2233 Patients With Myelofibrosis Treated With Ruxolitinib in the Expanded-Access JUMP Study. Blood (2023) 142 (Supplement 1): 5174.
- Haifa Kathrin Al-Ali, Ruben Mesa, J.E. Hamer-Maansson, Evan Braunstein, Claire Harrison. Effect of new or worsening anemia on clinical outcomes in patient with Myelofibrosis (MF) treated with ruxolitinib (RUX): a post hoc analysis of the COMFORT-I and -II trials. Abstract PB2185, Presented at EHA 2023.
433370/web/jak/04.24/0