Точная оценка маркеров системы комплемента в крови играет ключевую роль в диагностике и лечении нефрологических патологий. Понимание особенностей работы системы комплемента и ее влияния на течение заболеваний помогает врачам принимать обоснованные диагностические решения и подбирать наиболее адекватную терапию.
Пожалуйста, нажмите на интересующий вас раздел, чтобы его открыть.
Система комплемента
Система комплемента — это важный компонент врожденного иммунитета, играющий роль в защите организма от инфекций и регуляции воспалительных процессов. Работа системы комплемента связывает врожденный и приобретенный иммунитет благодаря участию в фагоцитозе, выработке антител, уничтожении чужеродных клеток. Гиперактивация системы комплемента лежит в основе патогенеза широкого спектра нефрологических заболеваний.
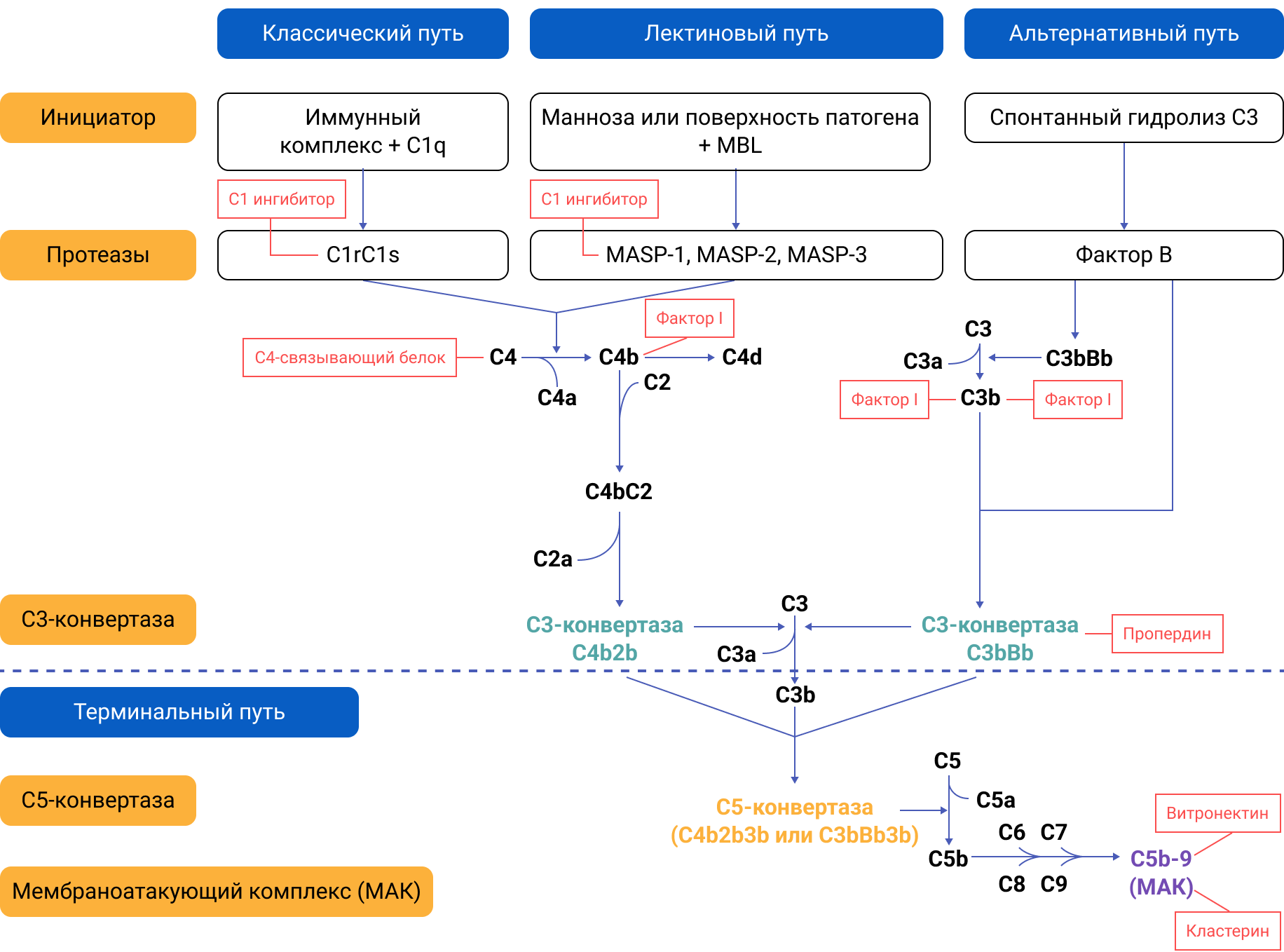
Система комплемента включает более 30 белков и их рецепторов, находящихся в крови и на поверхности клеток. Ее активация может происходить тремя путями (рис.1):
- Классическим (активация через комплекс антиген-антитело). Компоненты классического пути обозначаются буквой С и цифрой (от С1 до С9).
- Лектиновым (через маннозосвязывающий лектин — протеин сыворотки, связывающийся с маннозой, фруктозой или N-ацетилглюкозаминовыми группами на клеточных стенках бактерий и дрожжей или на вирусах).
- Альтернативным. Благодаря спонтанному гидролизу С3, не зависящему от наличия патогенных клеток, работает «вхолостую» постоянно. При контакте с поверхностью микроорганизмов или иммуноглобулинами активность системы резко возрастает за счет усиления в механизме амплификационной петли. Этот путь активации не требует участия антител.
Рисунок 1. Пути активации системы комплемента.
Конечной стадией активации комплемента по любому из трех путей является формирование мембраноатакующего комплекса (МАК), цитотоксического компонента системы комплемента, приводящего к лизису чужеродных клеток-мишеней.
Система комплемента участвует в дифференциации «своих» и «чужих» клеток, благодаря присутствию на собственных клетках организма регуляторных молекул, подавляющих активацию комплемента.
Активация системы комплемента происходит методом цепной реакции, что требует наличия достаточной концентрации каждого из ее компонентов. Активные формы компонентов системы комплемента существуют непродолжительное время и дезактивируются при отсутствии контакта с другими звеньями системы. Если концентрация компонента ниже пороговой, процесс активации системы будет остановлен.
Регуляция системы комплемента
Процесс осуществляется ингибиторами (такими как C1-ингибитор, факторы H и I), предотвращающими чрезмерную активацию и повреждение собственных тканей организма. Ингибитор С1 контролирует классический и лектиновый пути активации, ограничивая действие С4 и С2 с помощью связывания C1r- и С1s-протеаз.
С4-связывающий белок (C4BP) расщепляет С4 и помогает фактору I расщеплять C4b. Фактор H связывается с гликозаминогликанами, которые есть на собственных клетках, но не на клетках патогенов. Этот белок является кофактором фактора I. Кроме того, он ингибирует активность C3bBb. Фактор В — активатор альтернативного пути, запускающий образование С3-конвертазы.
Дисбаланс активирующих и ингибирующих факторов в системе комплемента, вызванный генетическими мутациями или нарушением регуляции, может способствовать развитию множества патологий.
Комплемент является важным аспектом защиты от инфекции, и регуляция активации системы комплемента тонко сбалансирована. В некоторых случаях функционирование системы нарушается, что приводит к неконтролируемой активации комплемента с образованием избыточного количества МАК.
Нарушение активности альтернативного пути комплемента может привести к развитию С3-гломерулопатии (C3ГП), которая характеризуется преимущественным отложением депозитов С3 в клубочках почек1.
Заболевания, связанные с изменением уровня системы комплемента
Гломерулярные заболевания являются одной из основных причин развития терминальной почечной недостаточности. Постановка точного диагноза на ранней стадии развития заболевания ведет к своевременному назначению эффективной терапии и способствует сохранению почечной функции. Золотым стандартом диагностики гломерулярной патологии является нефробиопсия.
Гиперактивация системы комплемента при гломерулярных заболеваниях приводит к более тяжелому течению заболевания и ускоряет прогрессирование почечной дисфункции. В связи с этим высокая степень вовлеченности гиперактивации комплемента в патологический процесс приводит к необходимости более быстрого принятия решения относительно диагностических активностей (проведение нефробиопсии), а также назначения терапии1,2.
Аномалии в системе комплемента связаны с воспалительными и аутоиммунными заболеваниями, к которым относятся:
- Комплемент-опосредованные гломерулопатии (например, C3-гломерулопатия);
- Иммунокомплексный мембранопролиферативный гломерулонефрит (ИК МПГН);
- IgA-нефропатия;
- Волчаночный нефрит (люпус-нефрит);
- Мембранозная нефропатия;
- Постинфекционный гломерулонефрит;
- Фокально-сегментарный гломерулосклероз (ФСГС);
- Тубулоинтерстициальный нефрит;
- Острая почечная недостаточность (острое поражение почек, ОПП);
- Реакции отторжения трансплантата.
Маркеры комплемента в клинической практике
Для оценки состояния системы комплемента наиболее часто применяются следующие маркеры3:
- C3 — один из ключевых белков системы комплемента. Он участвует в классическом и альтернативном путях активации, отвечает за устойчивость к бактериальным инфекциям, используется в опсонизации, повышает проницаемость сосудистой стенки, взаимодействует с иммунными комплексами.
- C4 — важный компонент системы комплемента, снижение которого в сыворотке крови указывает на активацию комплемента по классическому пути. Он способен активировать фагоцитоз, нейтрализацию вирусов, взаимодействие с иммунными комплексами. Снижение С4 является одним из диагностических маркеров аутоимунной патологии, например системной красной волчанки.
- CH50 — маркер активации системы комплемента по классическому пути, который позволяет оценить активность образования МАК, а также определить влияние гиперактивации системы комплемента по классическому пути на развитие гемолиза у пациента. Это полезный инструмент в рамках начального скрининга активности системы комплемента, поскольку для нормального результата требуется неповрежденная функциональная способность всех девяти компонентов классического пути.
- AP50 — маркер активности альтернативного пути. Он позволяет определить влияние гиперактивации системы комплемента по альтернативному пути на развитие гемолиза у пациента.
- C5a и C3a — анафилотоксины, активные фрагменты, образующиеся при активации системы комплемента, способствующие привлечению иммунокомпетентных клеток в очаг воспаления и выступающие как маркеры воспаления. Наиболее часто уровень С5а повышается в случае развития острых воспалительных реакций.
- MAК (мембраноатакующий комплекс) — показатель терминальной фазы активации комплемента. МАК индуцирует образование активных форм кислорода и эйкозаноидов, стимулирует реорганизацию цитоскелета, а также диссоциацию белков щелевой диафрагмы, что приводит к повреждению подоцита. В результате усиливается проницаемость гломерулярной капиллярной стенки и развивается протеинурия при формировании гломерулопатий.
Важно учитывать, что референсные значения маркеров различаются между лабораториями и странами, а также в научных публикациях, в том числе по единицам измерения (мг/дл, мг/мл, мкг, г/л). На это следует обращать внимание при интерпретации результатов.
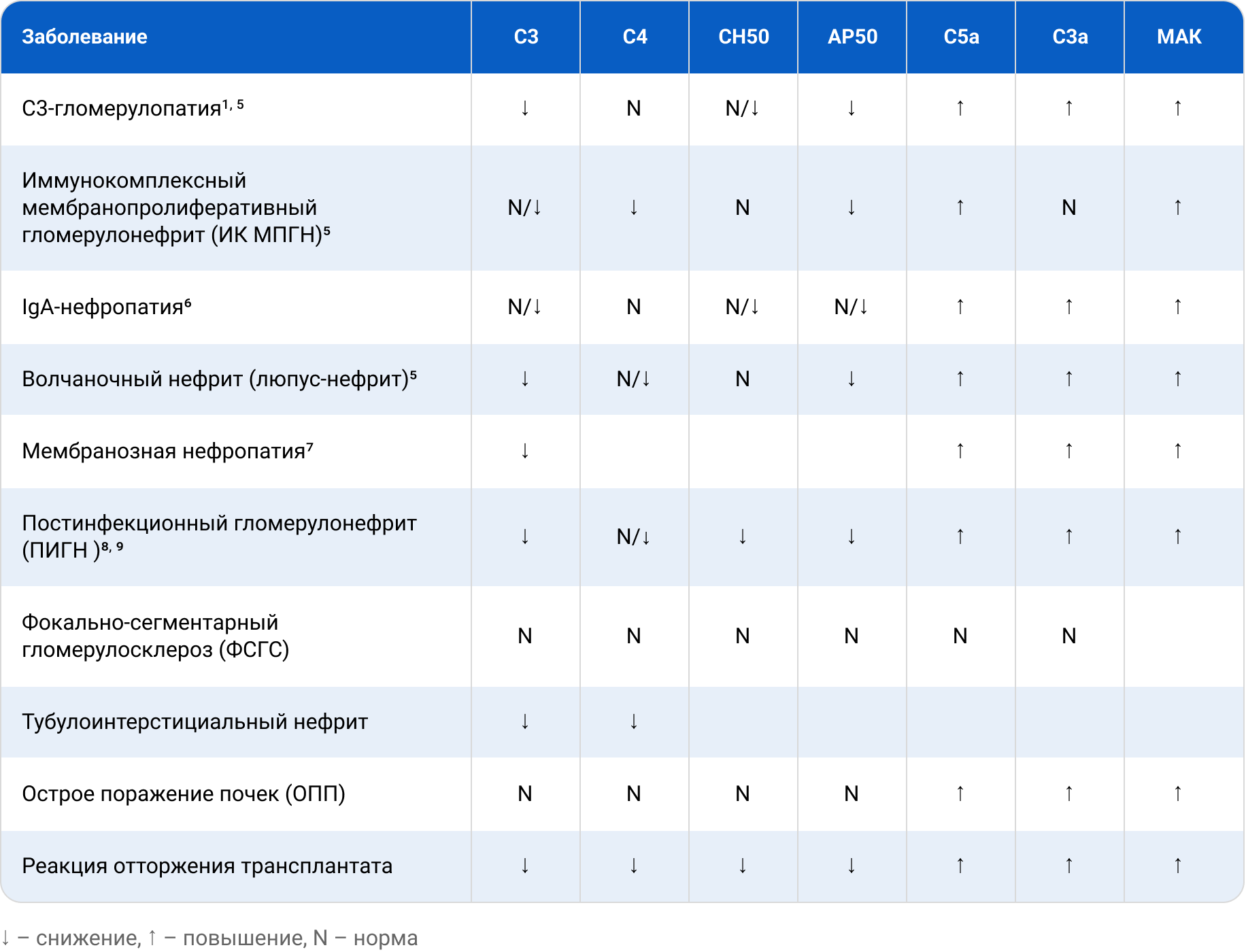
Хотя считается, что компоненты комплемента в основном синтезируются в печени и активируются в кровотоке, новые данные свидетельствуют о том, что некоторая их часть может синтезироваться и активироваться внутри почки, напрямую вызывая ее повреждение. Биомаркеры комплемента в моче, вероятно, лучше отражают патологические процессы, происходящие в почках, по сравнению с традиционными сывороточными биомаркерами комплемента, на которые может влиять системное воспаление. Кроме того, получение такого биоматериала для анализа является неинвазивным4. Необходимы дополнительные исследования для лучшего понимания роли идентификации компонентов комплемента в моче. В таблице 1 представлены возможные изменения маркеров системы комплемента при различных заболеваниях почек.
Таблица 1. Общее изменение маркеров комплемента при различных нефрологических заболеваниях.
Клинические рекомендации по диагностике маркеров комплемента10
В последние годы при диагностике и лечении гломерулярных заболеваний врачи все больше опираются на оценку маркеров системы комплемента. Эти маркеры играют ключевую роль в понимании патофизиологии различных гломерулярных состояний. Такая практика является проявлением более широкой тенденции перехода к персонализированной медицине, при которой маркеры комплемента могут помочь адаптировать стратегии лечения с учетом индивидуальных профилей пациентов.
Использование этих показателей для диагностики гломерулярных болезней входит в различные клинические рекомендации:
- Клинические практические рекомендации KDIGO 2021 по лечению гломерулярных болезней11.
- Клинические рекомендации «Мембранозная нефропатия» (2021 г.)12.
- Клинические практические рекомендации KDIGO 2021 по лечению волчаночного нефрита и др13.
Российский опыт
Согласно данным Н.Л. Козловской С3 и С4 компоненты системы комплемента позволяют судить о преимущественной активации комплемента по альтернативному или классическому пути. У большинства пациентов с С3-гломерулопатией отмечалось снижение функциональной активности С3, что авторы связывают с усиленным его потреблением при активации альтернативного пути. Для идиопатического мембранопролиферативного гломерулонефрита характерно сочетание активации альтернативного и классического путей комплемента, а для волчаночного нефрита IV класса — преимущественно классического пути, хотя содержание С3 и С4 в крови в большинстве случаев не изменяется21.
Важные моменты в диагностике нарушений работы системы комплемента
- Комплексная оценка. При подозрении на наличие патологии, связанной с нарушениями в системе комплемента, рекомендовано определять несколько маркеров для лучшего понимания пути гиперактивации и ее причин.
- Учет клинического контекста. Интерпретация результатов должна основываться на клинической картине и данных других лабораторных исследований.
- Использование биомаркеров. Это позволяет оценить эффективность терапии при аутоиммунных и воспалительных заболеваниях почек и способствует сокращению срока постановки диагноза, назначению таргетной терапии и повышению точности прогноза заболевания.
- Стандартизация. Использование одной лаборатории или единого стандарта для проведения исследований и оценки показателей.
Мониторинг С3 и С4 компонентов комплемента у пациентов с гломерулярными заболеваниями обеспечивает проведение ранней диагностики, подбор таргетной терапии и своевременную корректировку лечения.
Исследования показали, что снижение С3 в сыворотке крови часто ассоциируется с ИК МПГН, С3-гломерулопатией, ПИГН и волчаночным нефритом14, 15. Низкий уровень этого показателя может приводить к неблагоприятным исходам гломерулярных заболеваний, в т. ч. к развитию терминальной почечной недостаточности и смерти пациента16.
Пациенты с С3-гломерулопатией и низким уровнем С3 имели более тяжелое течение заболевания17. А в случае IgA-нефропатии включение компонентов С3 и C4 с высокой точностью подтверждает прогноз тяжелого течения заболевания18. Снижение С3 у пациентов с мембранозной нефропатией приводит к снижению общей и почечной выживаемости19.
Также низкий С3 может быть важным предиктором риска смерти и терминальной почечной недостаточности у пациентов с АНЦА-васкулитом20.
Определение маркеров системы комплемента — ценный инструмент в диагностике и мониторинге нефрологических заболеваний. Правильная интерпретация этих данных помогает точнее идентифицировать патологический процесс и оптимизировать лечение пациентов.
Список сокращений
- С1—С9 — компоненты классического пути системы комплемента;
- MAC, МАК — мембраноатакующий комплекс;
- C4BP — С4-связывающий белок;
- C3bBb — С3 конвертаза;
- C3GN — С3-гломерулонефрит;
- ИК МПГН — иммунокомплексный мембранопролиферативный гломерулонефрит;
- ФСГС — фокально-сегментарный гломерулосклероз;
- ОПП — острое поражение почек;
- CH50 — показатель общей гемолитической способности;
- AP50 — анализ активности альтернативного пути;
- C5a и C3a — анафилотоксины;
- ПИГН — постинфекционный гломерулонефрит;
- KDIGO — некоммерческое объединение, деятельность которого направлена на улучшение ухода и результатов лечения людей с заболеваниями почек во всем мире.
Источники
- Длин Владимир Викторович, Игнатова Майя Сергеевна Нефропатии, связанные с патологией системы комплемента // Рос вестн перинатол и педиат. 2016. №6. URL: https://cyberleninka.ru/article/n/nefropatii-svyazannye-s-patologiey-sis... (дата обращения: 25 ноября 2024 г.).
- Gunn W.C. The variation in the amount of complement in the blood in some acute infectious diseases and its relation to the clinical features. J Pathol Bacteriol 1915; 19: 155–181.
- Stefan P. Berger, Anja Roos, Mohamed R. Daha, Complement and the kidney: What the nephrologist needs to know in 2006?, Nephrology Dialysis Transplantation, Volume 20, Issue 12, December 2005, Pages 2613–2619, https://doi.org/10.1093/ndt/gfi166.
- Kesarwani V, Bukhari MH, Kahlenberg JM, Wang S. Urinary complement biomarkers in immune-mediated kidney diseases. Front Immunol. 2024 Jun 3;15:1357869. doi: 10.3389/fimmu.2024.1357869. PMID: 38895123; PMCID: PMC11184941.
- Юрова В. А., Боброва Л. А., Козловская Н. Л., Коротчаева Ю. В., Серова А. Г., Козлов Л. В., Андина С. С., Демьянова К. А., Кучиева А. М., Рощупкина С. В. ИЗМЕНЕНИЯ В СИСТЕМЕ КОМПЛЕМЕНТА ПРИ МЕМБРАНОПРОЛИФЕРАТИВНОМ ГЛОМЕРУЛОНЕФРИТЕ // Терапевтический архив. 2017. №6. URL: https://cyberleninka.ru/article/n/izmeneniya-v-sisteme-komplementa-pri-m... (дата обращения: 24 ноября 2024 г.).
- Caliskan Y, Kiryluk K. Novel biomarkers in glomerular disease. Adv Chronic Kidney Dis. 2014 Mar;21(2):205-16. doi: 10.1053/j.ackd.2013.12.002.
- Камышова Е.С., Семерюк Т.А., Бобкова И.Н. Современные представления о роли системы комплемента при мембранозной нефропатии. Терапевтический архив. 2022;94(6):772–776. DOI: 10.26442/00403660.2022.06.201563.
- Острый постстрептококковый (постинфекционный) гломерулонефрит [Текст] / А. В. Малкоч, А. Ю. Николаев, Н. Н. Филатова // Лечащий врач. - 2017. - ; №1. - С. 44-48.
- Гломерулонефрит (Нефритический синдром) Авторы:Frank O'Brien, MD, Washington University in St. Louis Справочник MSD.
- Нефрология. Клинические рекомендации / под ред. Е. М. Шилова, А. В. Смирнова, Н. Л. Козловской. - М. : ГЭОТАР-Медиа, 2016. - 816 с. - ISBN 978-5-9704-3714-8.
- Клинические практические рекомендации KDIGO 2021 по лечению гломерулярных болезней [Internet]. URL: https://kdigo.org/wp-content/uploads/2022/12/Russian-Translation-KDIGO-2... (дата обращения: 24 ноября 2024 г.).
- Клинические рекомендации Мембранозная нефропатия (2021 г.) [Internet]. URL: https://rusnephrology.org/wp-content/uploads/2024/06/%D0%9A%D0%A0_%D0%9C... (дата обращения: 24 ноября 2024 г.).
- Клинические практические рекомендации KDIGO 2021 по лечению волчаночного нефрита [Internet]. URL: https://kdigo.org/wp-content/uploads/2024/08/KDIGO-2024-Lupus-Nephritis-... (дата обращения: 24 ноября 2024 г.).
- Ali Mehdi, Jonathan J. Taliercio. C3 glomerulopathy. Cleveland Clinic Journal of Medicine June 2023, 90 (6 suppl 1) e1-e4;
- Rossi, G.M.; Ricco, F.; Pisani, I.; Delsante, M.; Maggiore, U.; Fiaccadori, E.; Manenti, L. C3 Hypocomplementemia Predicts the Progression of CKD towards End-Stage Kidney Disease in IgA Nephropathy, Irrespective of Histological Evidence of Thrombotic Microangiopathy. J. Clin. Med. 2024, 13, 2594.
- Vivarelli M, Barratt J, Beck LH Jr, Fakhouri F, Gale DP, Goicoechea de Jorge E, Mosca M, Noris M, Pickering MC, Susztak K, Thurman JM, Cheung M, King JM, Jadoul M, Winkelmayer WC, Smith RJH; for Conference Participants. The role of complement in kidney disease: conclusions from a Kidney Disease: Improving Global Outcomes (KDIGO) Controversies Conference. Kidney Int. 2024 Sep;106(3):369-391.
- Iatropoulos P, Daina E, Curreri M, Piras R, Valoti E, Mele C, et al. Cluster analysis identifies distinct pathogenetic patterns in C3 glomerulopathies/immune complex-mediated membranoproliferative GN. J Am Soc Nephrol. 2018;29:283–94.
- Tringali, E., Vetrano, D., Tondolo, F. et al. Role of serum complement C3 and C4 on kidney outcomes in IgA nephropathy. Sci Rep 14, 16224 (2024). https://doi.org/10.1038/s41598-024-65857-w.
- Tsai SF, Wu MJ, Chen CH. Low serum C3 level, high neutrophil-lymphocyte-ratio, and high platelet-lymphocyte-ratio all predicted poor long-term renal survivals in biopsy-confirmed idiopathic membranous nephropathy. Sci Rep. 2019 Apr 17;9(1):6209.
- Scurt FG, Hirschfeld V, Ganz M, Mertens PR, Chatzikyrkou C. Low levels of complement factor C3 at diagnosis can predict outcome in antineutrophil antibody associated vasculitis. J Nephrol. 2023 Nov;36(8):2281-2293. doi: 10.1007/s40620-023-01683-z. Epub 2023 Jul 7. PMID: 37418090.
- Козловская Н.Л., Юрова В.А., Козлов Л.В. и др. Функциональная активность С3 и С4 компонентов комплемента у пациентов с различными вариантами мембранопролиферативного гломерулонефрита. Клин фармакол и тер 2024; 33(3):31-35.
11334061/IPT/DIG/12.24