В 2024 году вышло два фундаментальных документа, которые подчеркивают важность системы комплемента в патогенезе заболеваний и выбора стратегии терапии пациентов с комплемент-опосредованными заболеваниями почек. Первый из них является обновленным анализом национального реестра редких заболеваний почек Великобритании (исследование RaDaR). Второй документ — это резолюция инициативы по улучшению глобальных исходов заболеваний почек (KDIGO — Kidney Disease: Improving Global Outcomes), которая была сформирована по итогам конференции «Роль комплемента в заболеваниях почек». Эти доклады имеют определяющее значение для поиска новых подходов и стратегий терапии пациентов с комплемент-опосредованными заболеваниями почек. Ниже представлена основная информация и заключения исследователей по данному вопросу.
Пожалуйста, нажмите на интересующий вас раздел, чтобы его открыть.
Основные заключения исследования реестра RaDaR 2024 года
В обновленном анализе исследования RaDaR, национального реестра редких заболеваний почек Великобритании, отмечено, что люди с редкими заболеваниями почек составляют 5—10% от общего числа пациентов с хронической болезнью почек, но среди них более 25% получают заместительную терапию почек3.
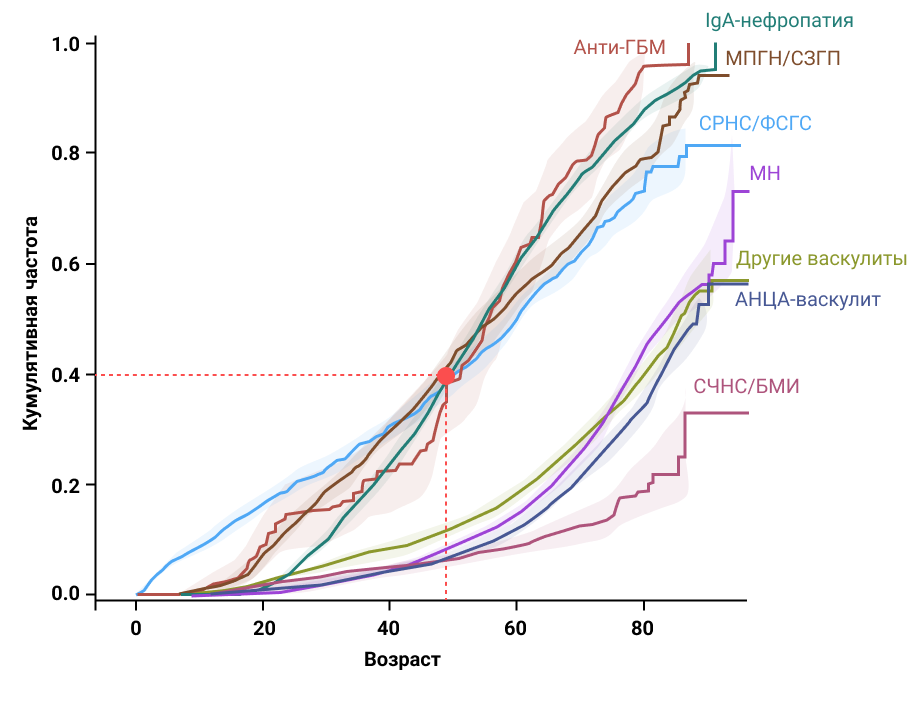
У 40% пациентов с IgA-нефропатией, ФСГС, МПГН/С3ГП, анти-ГБМ развивается ТПН к 50 годам3.
Авторы исследования пришли к заключению, что пациенты с редкими заболеваниями почек отличаются от общей популяции пациентов с ХБП: у них выше 5-летние показатели почечной недостаточности, но при этом выше выживаемость по сравнению с другими пациентами на стадиях 3—5 ХБП, поэтому их больше в когорте пациентов, нуждающихся в ЗПТ. Удовлетворение терапевтических потребностей пациентов с редкими заболеваниями почек может оказать значительное положительное влияние на долгосрочный спрос на ЗПТ3.
Резолюция KDIGO 2024: предпосылки
Неконтролируемая активация системы комплемента может вызывать или усугублять повреждение клубочков при различных заболеваниях почек. Хотя активация комплемента играет причинную роль в развитии аГУС и C3ГП, за последнее десятилетие появилось множество данных, подтверждающих участие комплемента в патогенезе других заболеваний почек, включая диабетическую нефропатию и различные формы гломерулонефритов. Одновременно увеличилось количество доступных видов и стратегий ведения пациентов, направленных на ингибирование системы комплемента.
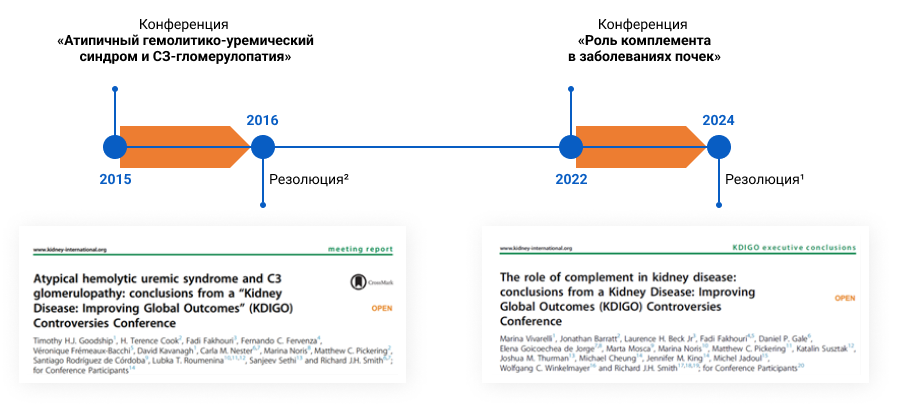
В 2022 году инициатива по улучшению глобальных исходов заболеваний почек (KDIGO — Kidney Disease: Improving Global Outcomes) провела конференцию по спорным вопросам. Участники конференции обсудили растущую роль системы комплемента в патофизиологии, диагностике и лечении различных гломерулярных заболеваний, диабетической нефропатии и атипичного гемолитико-уремического синдрома. В ходе мероприятия был проведен обзор доказательств, подтверждающих первичную и вторичную роли системы комплемента в прогрессировании различных заболеваний. Также были обсуждены значение биомаркеров для мониторинга течения заболевания и роль этапа клубочковой фильтрации в системе комплемента1.
В 2015 году KDIGO провела конференцию, где рассматривались спорные вопросы, касающиеся двух заболеваний почек, связанных с активацией комплемента: аГУС и С3ГП. С тех пор появились доказательства, подтверждающие роль комплемента в развитии и прогрессировании более широкого спектра почечных заболеваний, включая диабетическую нефропатию и различные формы гломерулонефритов. Дисфункция комплемента может выступать как первопричиной, так и вторичным фактором, усугубляющим прогрессию этих заболеваний. Почки представляют собой основную мишень для нарушений регуляции комплемента. Системные генетические дефекты в белках, регулирующих комплемент, могут вызывать изолированные нефропатии. При этом многие формы заболеваний почек вовлекают все пути системы комплемента. Уникальная восприимчивость почек к повреждениям, связанным с комплементом, может объясняться несколькими факторами, включая высокое гидростатическое давление в клубочках и фильтрацию плазмы в капиллярах гломерул, что приводит к гиперконцентрациям белков комплемента в непосредственной близости от ГБМ. Кроме того, наличие фенестраций в эндотелиальных клетках клубочков может облегчать доступ крупных белков плазмы к базальной мембране. Важно отметить, что базальная мембрана клубочков не экспрессирует внутренних регуляторов комплемента, которые присутствуют на эндотелиальных клетках, что также способствует повышенной уязвимости почек к повреждениям, вызванным активацией комплемента1.
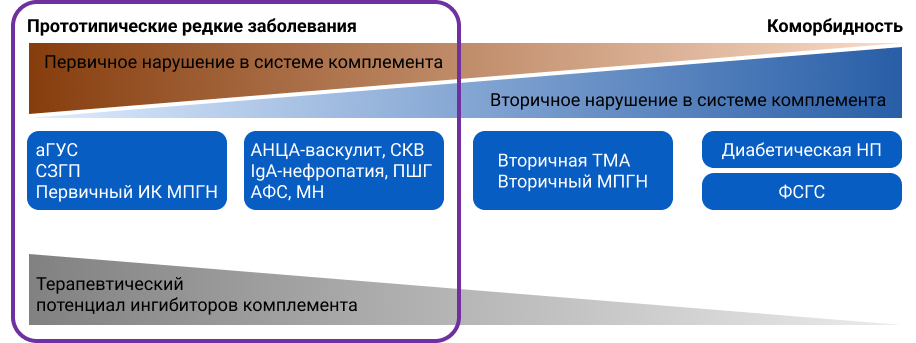
Резолюция KDIGO 2024: комплемент-опосредованные заболевания и коморбидность
Гломерулярные патологии, вызванные нарушением регуляции комплемента, представляют собой широкий спектр заболеваний, включающих как редкие, но прототипические комплемент-опосредованные заболевания, такие как аГУС и С3ГП, так и более сложные многофакторные заболевания, в которых активация комплемента может играть второстепенную роль, усугубляя тяжесть болезни. Роль комплемента требует дальнейшего подтверждения через клинические испытания и исследования биомаркеров системы комплемента. Среди таких заболеваний можно выделить АНЦА-васкулит, АФС, ФСГС, МПГН, IgA-нефропатию, ИК МПГН, МН и ТМА.
Резолюция KDIGO 2024: роль системы комплемента в патогенезе заболеваний и его влияние на выбор подхода к терапии комплемент-опосредованных заболеваний
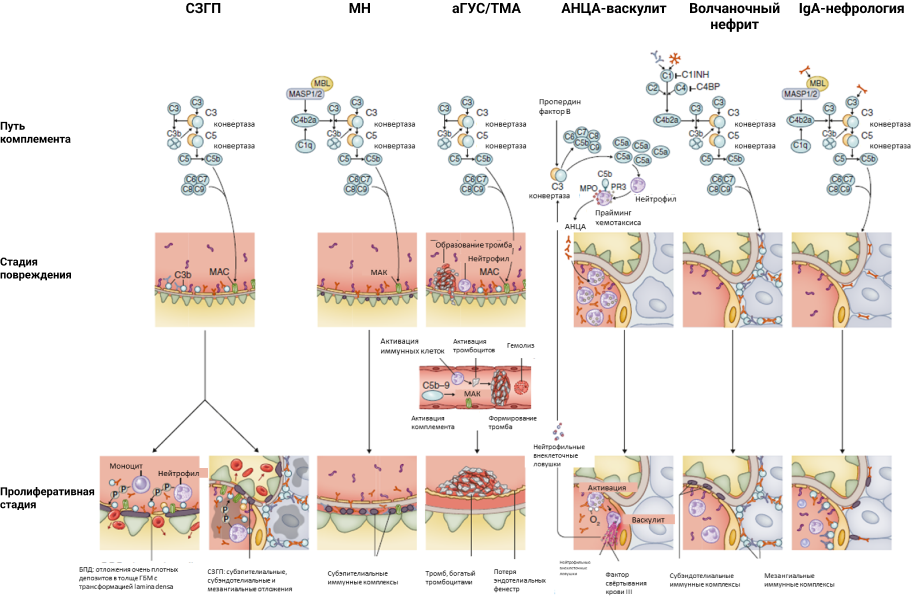
Роль системы комплемента при различных заболеваниях почек, согласно резолюции KDIGO 20241
Cистема комплемента постоянно активна из-за медленного спонтанного распада фракции C3. Активирующие компоненты комплемента не способны различать собственные клетки организма и чужеродные агенты, поэтому здоровье человека зависит от белков-регуляторов активации комплемента, которые предотвращают повреждения, вызванные комплементом. Для представленных на схеме гломерулярных заболеваний основным фактором является активация определенного пути, которая приводит к повреждению, переходящему в пролиферативную фазу поражения гломерул. С появлением все большего числа терапевтических агентов, нацеленных на разные части комплементной каскадной системы, становится критически важным понимать, как активация комплемента способствует развитию этих заболеваний. Это знание необходимо для правильного применения новых препаратов с целью улучшения исходов лечения пациентов.
Категоризация клинических параметров на основании консенсуса экспертов KDIGO 20241
Резолюция KDIGO 2024: новые горизонты клинических исследований и поиска новых групп препаратов
Многочисленные данные свидетельствуют о том, что активация или нарушение в работе системы комплемента играет важную роль в патогенезе все более широкого спектра заболеваний почек. Хотя при аГУС и С3ГП дисрегуляция альтернативного пути комплемента, по‑видимому, является основным патогенетическим фактором заболевания, в других состояниях комплемент может играть более сложную роль. Например, он может вызывать повреждение клубочков после отложения иммунных комплексов, как это наблюдается при МН, или способствовать хроническому повреждению, как при диабетической НП или ФСГС. Поскольку сейчас исследуется множество терапевтических агентов, нацеленных на различные участки каскада комплемента, расширяются знания о значении и месте каждого из белков в системе комплемента, а также его роли в развитии острого и хронического воспаления. В этой связи ключевым аспектом являются исследования панелей биомаркеров, специфичных для того или иного заболевания, которые могут облегчить предикцию, диагностику, мониторинг лечения и (или) оценку статуса различных гломерулярных заболеваний1.
Список сокращений
- KDIGO (Kidney Disease: Improving Global Outcomes) — инициатива по улучшению глобальных исходов заболеваний почек;
- RaDaR (The National Registry of Rare Kidney Diseases) — национальный реестр редких заболеваний почек Великобритании;
- IgA — иммуноглобулин A;
- ФСГС — фокально-сегментарный гломерулосклероз;
- МПГН — мембранопролиферативный гломерулонефрит;
- ИК МПГН — иммунокомплексный мембранопролиферативный гломерулонефрит;
- С3ГП — С3-гломерулопатия;
- ГБМ — гломерулярная базальная мембрана;
- ТПН — терминальная почечная недостаточность;
- СРНС — стероид-резистентный нефротический синдром;
- АНЦА — антитела к цитоплазме нейтрофилов;
- МН — мембранозная нефропатия;
- СЧНС — стероид-чувствительный нефротический синдром;
- БМИ — болезнь минимальных изменений;
- ХБП — хроническая болезнь почек;
- ЗПТ — заместительная почечная терапия;
- аГУС — атипичный гемолитико-уремический синдром;
- АФС — антифосфолипидный синдром;
- ПШГ — пурпура Шенлейна-Геноха;
- ТМА — тромботическая микроангиопатия;
- НП — нефропатия;
- БПД — болезнь плотных депозитов;
- МАК — мембраноатакующий комплекс;
- СКВ — системная красная волчанка;
- рСКФ — расчетная скорость клубочковой фильтрации.
Источники
- Vivarelli M, et al. The role of complement in kidney disease: conclusions from a Kidney Disease: Improving Global Outcomes (KDIGO) Controversies Conference. Kidney Int. 2024 Jun 4:S0085-2538(24)00389-2. doi: 10.1016/j.kint.2024.05.015. Epub ahead of print. PMID: 38844295.
- Goodship TH, et al. Atypical hemolytic uremic syndrome and C3 glomerulopathy: conclusions from a "Kidney Disease: Improving Global Outcomes" (KDIGO) Controversies Conference. Kidney Int. 2017 Mar;91(3):539-551. doi: 10.1016/j.kint.2016.10.005. Epub 2016 Dec 16. PMID: 27989322.
- Wong K., Pitcher D., Braddon F., et al. Effects of rare kidney diseases on kidney failure: a longitudinal analysis of the UK National Registry of Rare Kidney Diseases (RaDaR) cohort. Lancet. 2024; 403: 1279–89.
11277209/IPT/DIG/09.24/0