Резюме
- Недостаточное снижение уровня эстрогена (эстрон (E1) ≥1,3 пг/мл и/или эстрадиол (E2) ≥0,5 пг/мл) связано с трехкратным увеличением риска прогрессирования раннего РМЖ1.
- У 30% пациенток, принимавших стандартную дозу анастрозола (1 мг/день), уровни эстрогенов оказались выше пороговых значений (E1 ≥1,3 пг/мл и/или E2 ≥0,5 пг/мл)2.
- Высокие дозы анастрозола (10 мг/день) привели к подавлению E1 и E2 ниже пороговых значений у большинства (76%) пациенток, приверженных терапии2.
- Адекватное подавление эстрогенов сохранялось или достигалось у 91,3% пациенток при переходе с высокой дозы анастрозола (10 мг/день) на стандартную дозу летрозола (2,5 мг/день)2.
Введение
Ингибиторы ароматазы (ИА) анастрозол, экземестан и летрозол играют важную роль в лечении женщин в постменопаузе с ранним гормонозависимым раком молочной железы (ER+ РМЖ), ингибируяароматазу — фермент, который преобразует ангдрогенные предшественники в эстрогены (эстрон (E1) и эстрадиол (E2)).
Несмотря на то, что все три ИА демонстрируют сходную клиническую эффективность, оказалось, что недостаточное подавление экспрессии эстрогенов (E1 ≥1,3 пг/мл и/или E2 ≥0,5 пг/мл) у пациенток в постменопаузе, принимавших анастрозол, связано со статистически значимым трехкратным увеличением риска прогрессирования РМЖ1. Такая связь не была обнаружена для пациенток, принимавших экземестан или летрозол.
В 2024 г. в Journal of Clinical Cancer Research опубликованы результаты проспективного фармакодинамического исследования, основной целью которого было определить долю женщин, у которых наблюдается недостаточное подавление продукции эстрогенов после 8–10 недель стандартной адъювантной терапии анастрозолом, и оценить эффективность и безопасность высокой дозы анастрозола (10 мг/день) у таких пациенток2. Эта работа имеет потенциально важное практическое значение для применения ИА у больных РМЖ.
Пациенты и методы исследования
Критерии включения
В исследование включали женщин в постменопаузе с I–III стадией ER+ HER2 — РМЖ после завершения хирургического лечения, адъювантной лучевой и химиотерапии. Женщины в возрасте <60 лет, у которых не было предшествующей двусторонней овариэктомии, включались в исследование при условии наличия аменореи в течение >12 месяцев и уровня фолликулостимулирующего гормона (ФСГ) в постменопаузальном диапазоне (для тех, кто получил (нео)адъювантную химиотерапию, этот критерий должен был быть соблюден на момент постановки диагноза). ER+ заболевание как ≥1% клеток с положительным окрашиванием ядер.
Определения
- Приверженность лечению: документально подтверждённый (дневник приёма) прием не менее 80% запланированной дозы лекарства в течение 45–84 дней.
- Высокий уровень эстрогенов: Е1 ≥1,3 пг/мл и/или Е2 ≥0,5 пг/мл.
- Низкий уровень эстрогенов: Е1 <1,3 пг/мл и/или Е2 <0,5 пг/мл.
Дизайн исследования
В исследование включались пациентки, проходившие лечение в филиалах клиники Майо (США) с 2020 по 2022 годы.
Первый цикл лечения (цикл 1: ANA1) предполагал получение пациентками анастрозола, вводимого по 1 мг перорально один раз в день в течение 8–10 недель. Образцы крови брались до начала и после завершении цикла 1 (ANA1) для определения уровней E1 и E2 в плазме. Если E1 был <1,3 пг/мл и/или E2 <0,5 пг/мл после ANA1, пациентка прекращала участие в исследовании, поскольку достигала адекватного снижения уровня эстрогенов. Дальнейшее лечение оставалось на усмотрение пациента и их лечащих врачей.
Пациентки с неадекватным подавлением продукции эстрогенов после цикла 1 (ANA1) имели возможность либо выйти из исследования, либо перейти ко второму циклу лечения. Цикл 2 (ANA10) предполагал получение анастрозола в дозе 10 мг перорально один раз в день в течение ещё 8–10 недель. Во втором цикле оценивали, приведет ли повышенная доза анастрозола к адекватному снижению уровня эстрогенов.
Независимо от уровней E1 и E2, достигнутых после завершения второго цикла (ANA10), все пациентки переводились на цикл 3 лечения: 8–10 недель летрозола по 2,5 мг перорально один раз в день. После завершения третьего цикла определяли уровни E1 и E2. Затем пациентки прекращали свое участие в исследовании, и дальнейшее лечение оставалось на усмотрение пациентов и их лечащих врачей.
Результаты
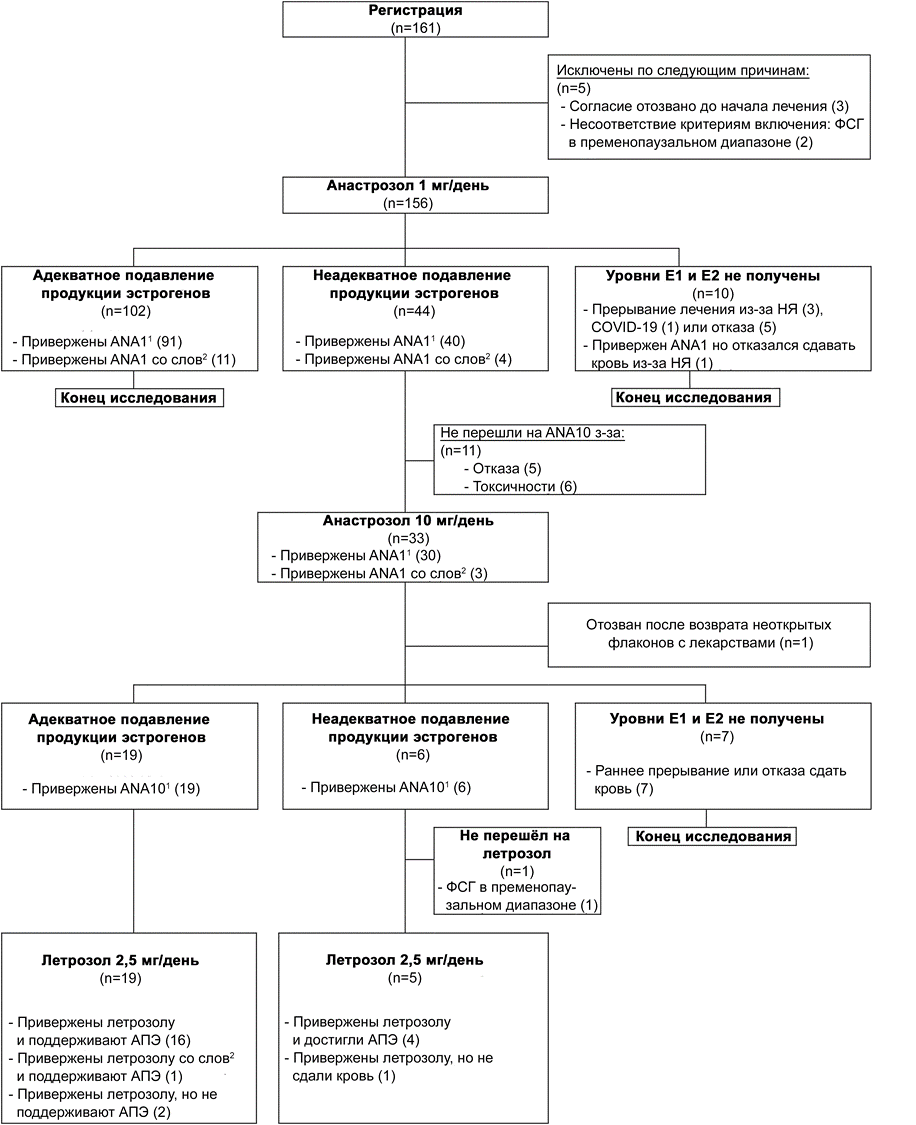
Прохождение пациентками трех циклов лечения по протоколу исследования представлено на рис. 1. Всего в исследование была зарегистрирована 161 пациентка, из которых 156 пациенток начали первый цикл лечения (ANA1). До начала лечения практически у всех пациенток (97,4%, n=152) наблюдались высокие уровни E1 и E2.
ANA1
Достичь низкого уровня эстрогенов после ANA1 смогли 65,4% (n=102) пациенток, не достигли 28,2% (n=44) пациенток, и у 6,4% (n=10) пациенток оценка не проводилась. В когорте пациенток, приверженных лечению (n=132), низкого уровня эстрогенов достигли 68,9% (n=91), не достигли 30,3% (n=40); и у одной (0,8%) пациентки уровень эстрогена не оценивался.
ANA10
В цикл 2 (ANA10) перешли 33 пациентки с недостаточно низким уровнем эстрогена, из которых 30 пациенток были привержены предшествующему лечению ANA1 (рис. 1).
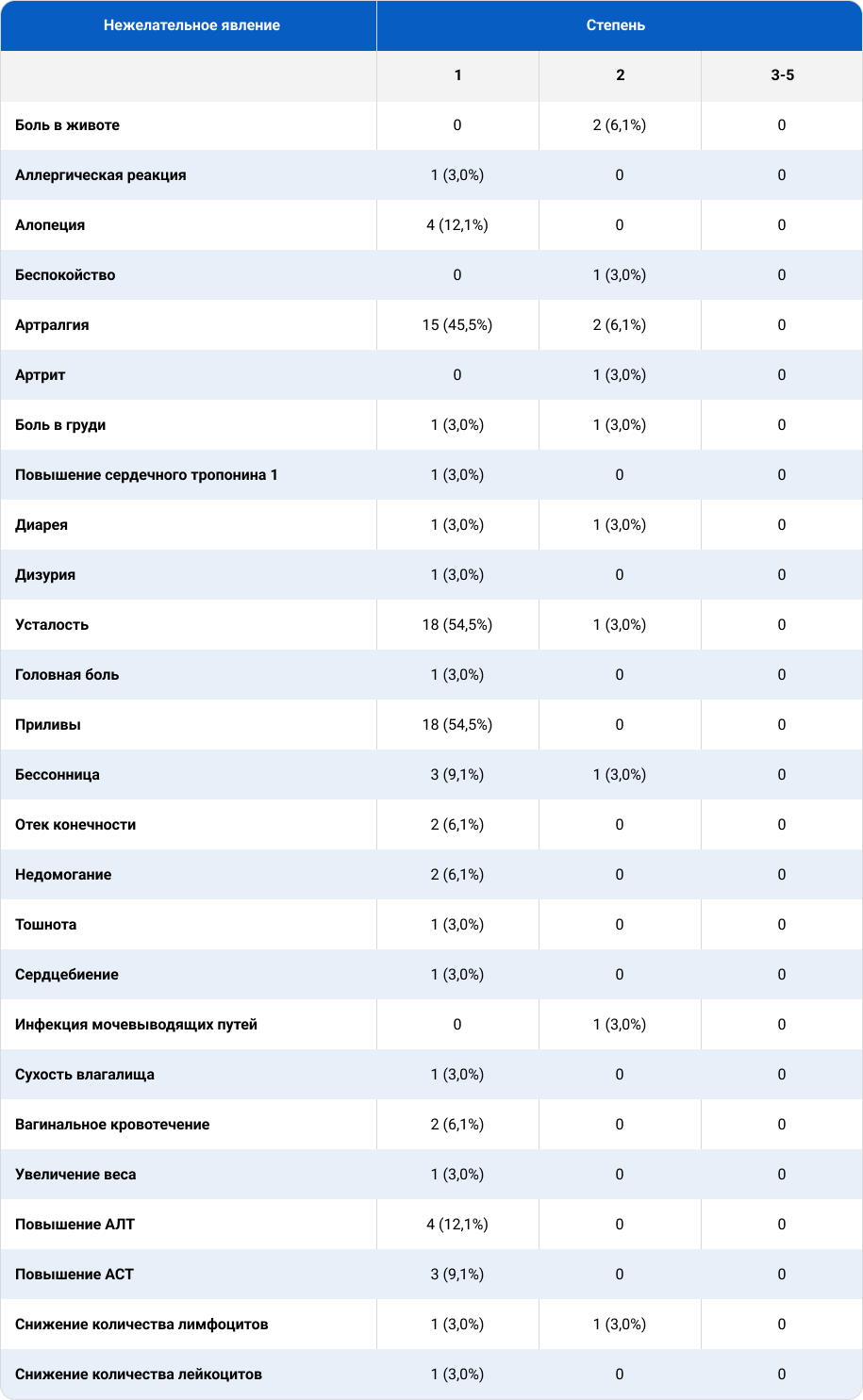
Из 33 пациенток, начавших цикл 2 (ANA10), только две досрочно прекратили прием лекарства из-за нежелательных явлений (НЯ). Тяжёлые НЯ (степени 3–5) в период приёма 10 мг/день анастрозола зарегистрированы не были (табл. 2). Адекватное снижение уровня эстрогенов после ANA10 было достигнуто у 59,4% (n=19) пациенток, в то время 18,8% (n=6) не достигли низкого уровня. У семи пациенток (21,9%) уровень эстрогена не оценивался. Таким образом, частота достижения низкого уровня эстрогенов после ANA10 составила 59,4% (90% ДИ, 43,4%–74,0%).
В когорте пациенток, приверженных лечению ANA10 (n=25), низкого уровня эстрогена достигли 19 человек (76,0%; 90% ДИ, 58,1%–89,0%), и шесть (24,0%) пациенток не смогли достичь низкого уровня.
Летрозол, 2,5 мг/день
Все пациенты, завершившие ANA10, имели право перейти в третий цикл на терапию летрозолом (2,5 мг/день, 8–10 недель). Приём летрозола начали 24 пациентки, и никто из них не прекратил лечение досрочно. В когорте пациенток, приверженных лечению (n=23), 91,3% (n=21) пациенток сохранили или достигли низкий уровень эстрогена (рис. 1).
Заключение
В представленном фармакодинамическом исследовании было продемонстрировано, что примерно у 30% женщин в постменопаузе с операбельным ER+ HER2 — РМЖ, принимавших стандартную дозу анастрозола (1 мг/день), наблюдалось недостаточное подавление продукции эстрогенов (E1 ≥1,3 пг/мл и E2 ≥0,5 пг/мл)2. Среди тех пациенток, которые перешли на высокую дозу анастрозола (10 мг/день) и были привержены лечению, 76% достигли низкого уровня эстрогенов2. Использование легкодоступных биомаркеров (E1 и E2) открывает возможности для индивидуального подбора дозировки анастрозола и улучшения результатов лечения женщин в постменопаузе с ER+ HER2-РМЖ. Авторы статьи отмечают, что необходимы дальнейшие исследования для определения клинической пользы от перехода на высокую дозу анастрозола (10 мг/день) или альтернативный ИА (летрозол).
Рисунок 1. Диаграмма прохождения пациентками трех циклов лечения по протоколу исследования2.
Сноски:
1приверженность лечению документально подтверждена записями в дневнике (прием не менее 80% запланированной дозы в течение 45–84 дней), предоставлен образец крови для тестирования E1 и E2;
2приверженность лечению со слов пациента, документально не подтверждена, но предоставлен образец крови для тестирования E1 и E2.
Таблица 1. Все НЯ, зарегистрированные в течение периода ANA10 (анастрозол, 10 мг/день перорально в течение 8–10 недель), независимо от их причины2.
Список сокращений
- ANA1 – цикл 1: анастрозол 1 мг/день;
- ANA10 – цикл 2: анастрозол 10 мг/день;
- ФСГ – фолликулостимулирующий гормон.
Список литературы
- Ingle JN, Cairns J, Suman VJ, et al. Anastrozole has an association between degree of estrogen suppression and outcomes in early breast cancer and is a ligand for estrogen receptor α. Clin Cancer Res. 2020;26:2986–96. https://doi.org/10.1158/1078-0432.CCR-19-3091
- Haddad ТC, Suman VJ, Giridhar RV, et al. Anastrozole dose escalation for optimal estrogen suppression in postmenopausal earlystage breast cаncer: a prospective trial. Clin. Cancer Res. 2024; 30: 3147-56. https://doi.org/10.1158/1078-0432.CCR-24-0341
11328340/RIB/web/12.24/0