Введение
Несмотря на эффективность современных вариантов адъювантной эндокринной терапии (ЭТ), риск рецидивирования все еще остается актуальной проблемой для пациентов с люминальным HER2− негативным раком молочной железы (РМЖ)1–4.
К настоящему времени два рандомизированных клинических исследования 3 фазы показали значительное улучшение выживаемости без признаков инвазивного заболевания (ВБИЗ) при использовании в адъюванте ингибиторов CDK4/6 у пациентов с HR+ HER2− ранним РМЖ. В исследовании NATALEE рибоциклиб в сочетании с нестероидными ингибиторами ароматазы (ИА) продемонстрировал статистически значимое улучшение ВБИЗ по сравнению с монотерапией ИА: ОР 0,715 (95% ДИ: 0,609–0,840), номинальный P < 0,0001, медиана наблюдения 44,2 мес.5–7 В исследовании monarchE комбинация абемациклиб + ЭТ также продемонстрировала статистически значимое улучшение ВБИЗ по сравнению с моноЭТ: ОР 0,680 (95% ДИ: 0,599–0,772); номинальный P < 0,001; медиана наблюдения 54 мес.8–10 Эксперты отмечали, что из-за различий в критериях включения исследование NATALEE охватило более широкую популяцию пациентов с HR+ HER2− ранним РМЖ, чем исследование monarchE5,11.
Представленное на конгрессе SABCS исследование реальной клинической практики показывает частоту рецидива у пациентов, соответствующих критериям включения в исследования NATALEE и monarchE, на фоне проведения современной адъювантной терапии.
Методы
Исследование основано на анализе данных электронных медицинских карт пациентов из базы Flatiron Health (США) за период с января 2011 по май 2024 года14. В анализ были включены пациенты в возрасте ≥ 18 лет с I–III стадией HR+ HER2− РМЖ на момент постановки диагноза, которые перенесли операцию и начали адъювантную ЭТ. В исследование включали пациентов, отвечавших критериям соответствия любого из исследований (NATALEE или monarchE) (рис. 1).
Результаты пациентов оценивали по следующим конечным точкам, измеряемым от даты операции:
- Безрецидивная выживаемость (БРВ): время до первого инвазивного ипсилатерального рецидива РМЖ, инвазивного локорегионального рецидива, отдаленного рецидива или смерти по любой причине*;
- Выживаемость без отдаленных метастазов РМЖ (ВБОМРМЖ): время до отдаленного рецидива РМЖ или смерти по любой причине;
- Общая выживаемость (ОВ): время до смерти по любой причине.
* — БРВ идентичен ВБИЗ (выживаемость без инвазивного заболевания), за исключением инвазивного контралатерального РМЖ и событий второго первичного инвазивного рака (не РМЖ) (согласно STEEP 2.0).
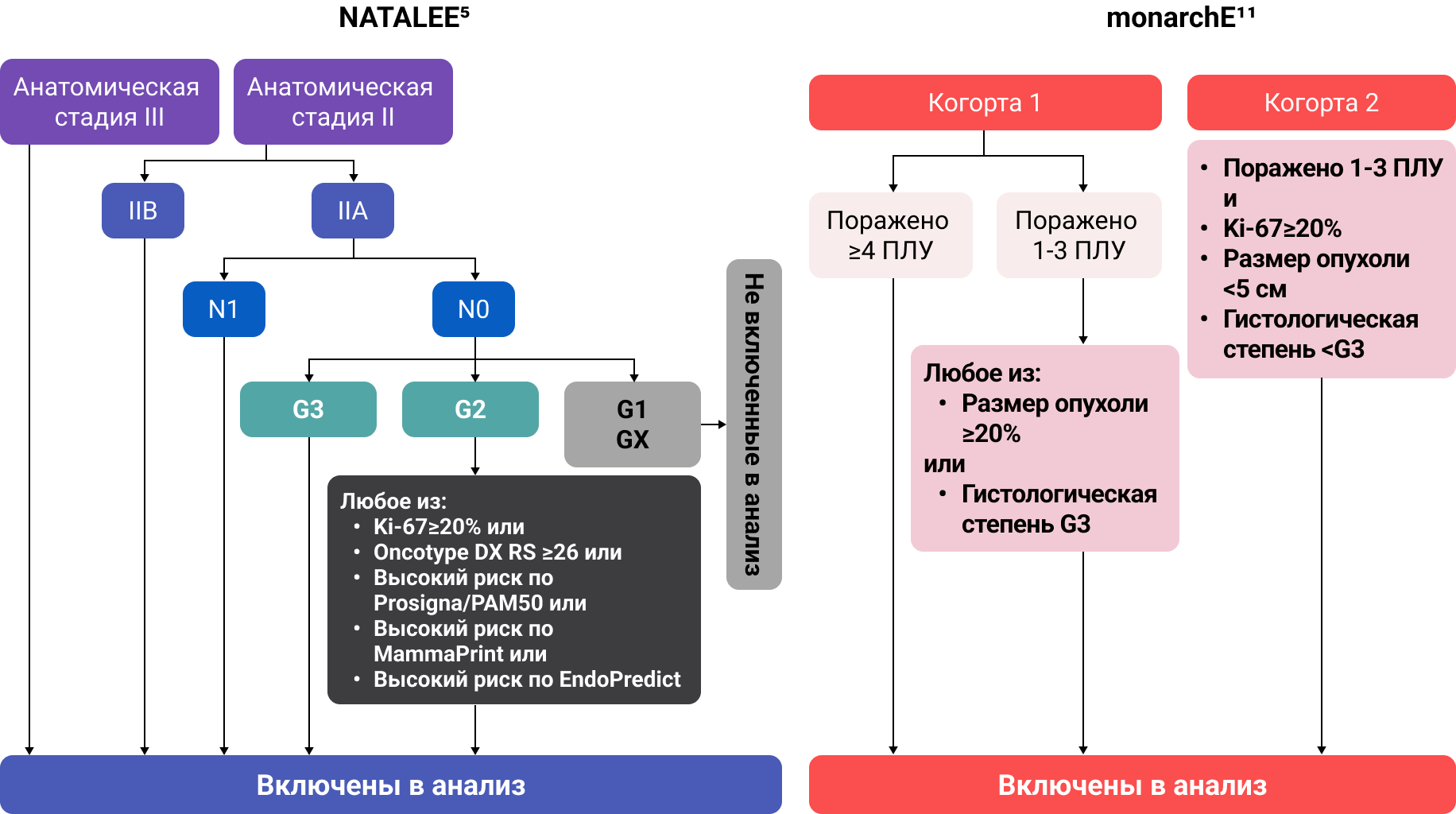
Рисунок 1. Критерии соответствия исследованиям NATALEE и monarchE для включения пациентов в анализ14
ПЛУ — подмышечный лимфатический узел; G — гистологическая степень злокачественности; N0 — 0 положительных лимфатических узлов; N1 — 1-3 положительных лимфатических узла; PAM50, Oncotype DX RS, MammaPrint, EndoPredict – методы геномного тестирования.
Результаты
Характеристики пациентов, заболевания и предшествующего лечения в когортах, соответствующих критериям включения в исследования NATALEE и monarchE
В общей сложности 7481 пациент соответствовал критериям отбора и был включен в анализ. Из них 33,9% (2534/7481) пациентов соответствовали критериям NATALEE и 15,5% (1157/7481) – критериям monarchE.
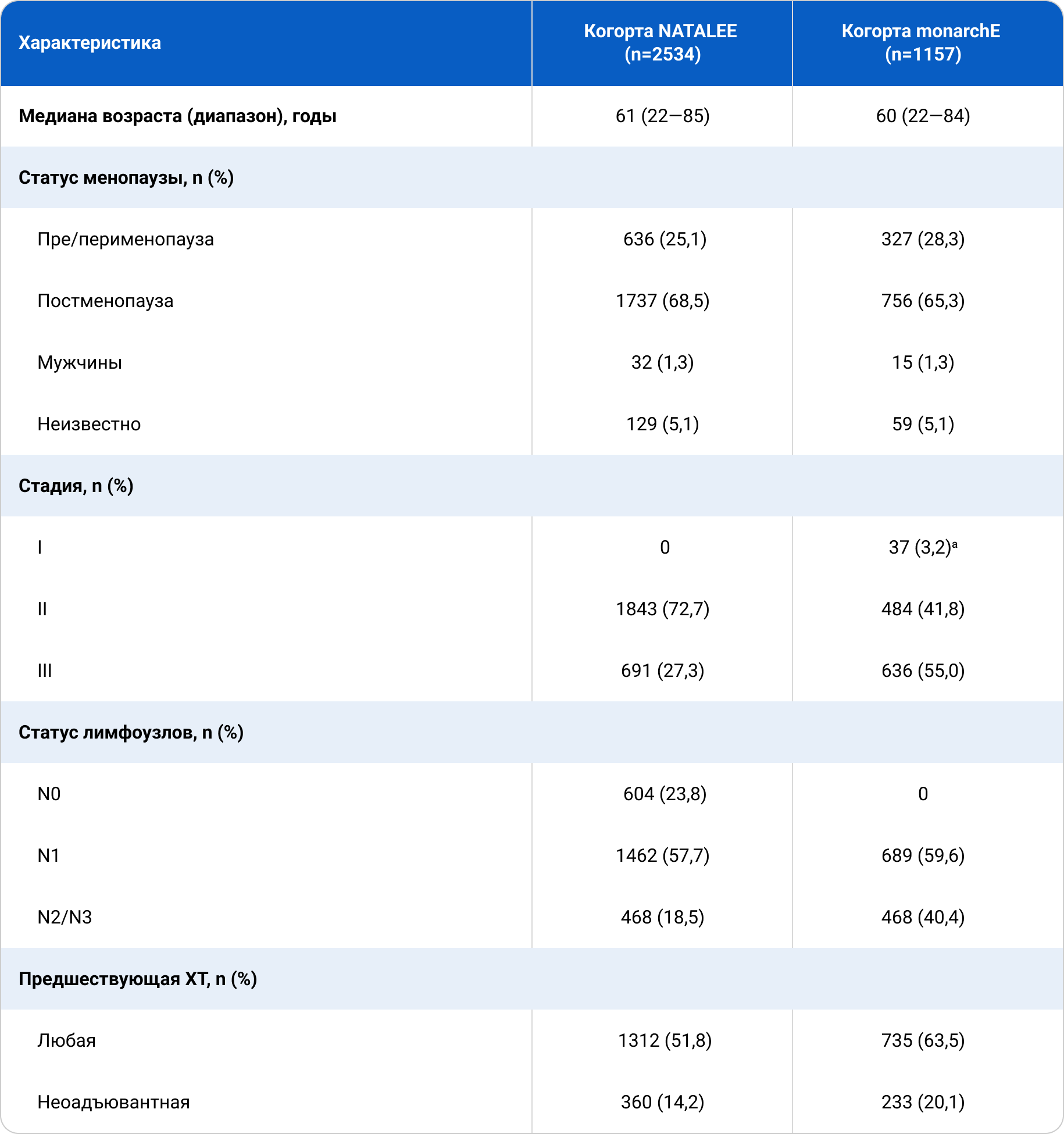
Возраст и менопаузальный статус были схожи между этими двумя когортами пациентов (табл. 1). Меньшее количество пациентов получили предшествующую химиотерапию (ХТ) в когорте, соответствующей критериям NATALEE (1312 [51,8%]), чем в когорте, соответствующей критериям monarchE (735 [63,5%]). Медиана наблюдения составила 55,1 мес. для пациентов когорты NATALEE и 53,4 мес. для пациентов когорты monarchE.
Таблица 1. Исходные характеристики пациентов, соответствующих критериям включения в исследования NATALEE и monarchE
a — Все T1N1mi.
Риск рецидива и смертность в когортах, соответствующих критериям включения в исследования NATALEE и monarchE
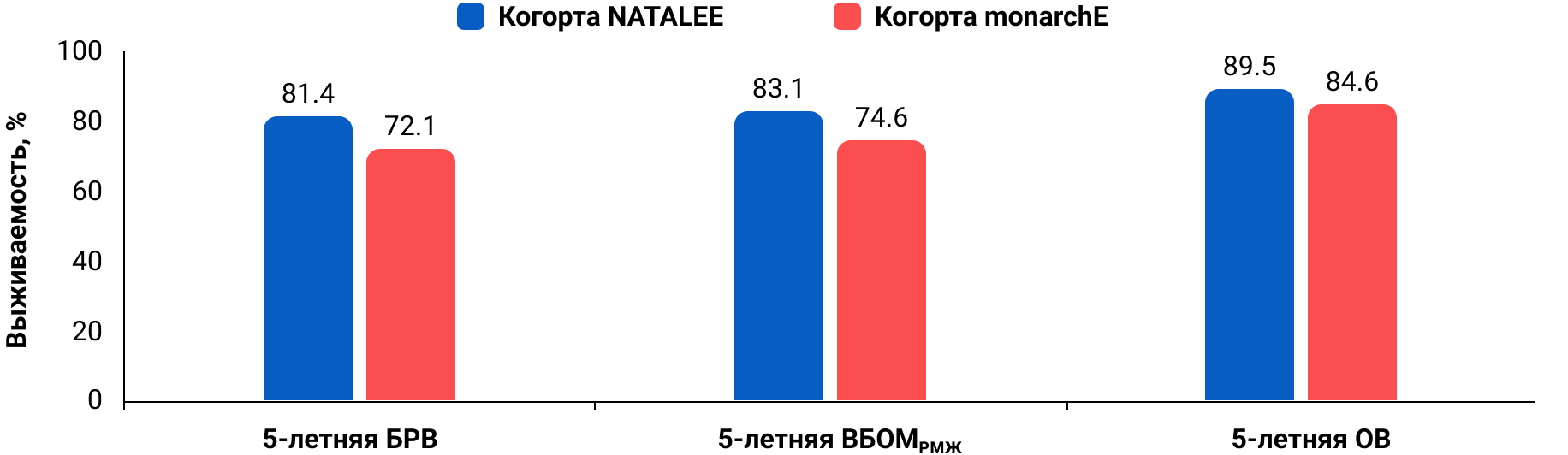
БРВ, ВБОМРМЖ и ОВ в когортах NATALEE и monarchE, полученные в ходе исследования, указывают на клинически значимые риски рецидива и смерти в течение 5 лет, несмотря на проводимую ЭТ (рис. 2).
Рисунок 2. 5—летние риски рецидива и смерти в когортах, соответствующих критериям NATALEE и monarchE
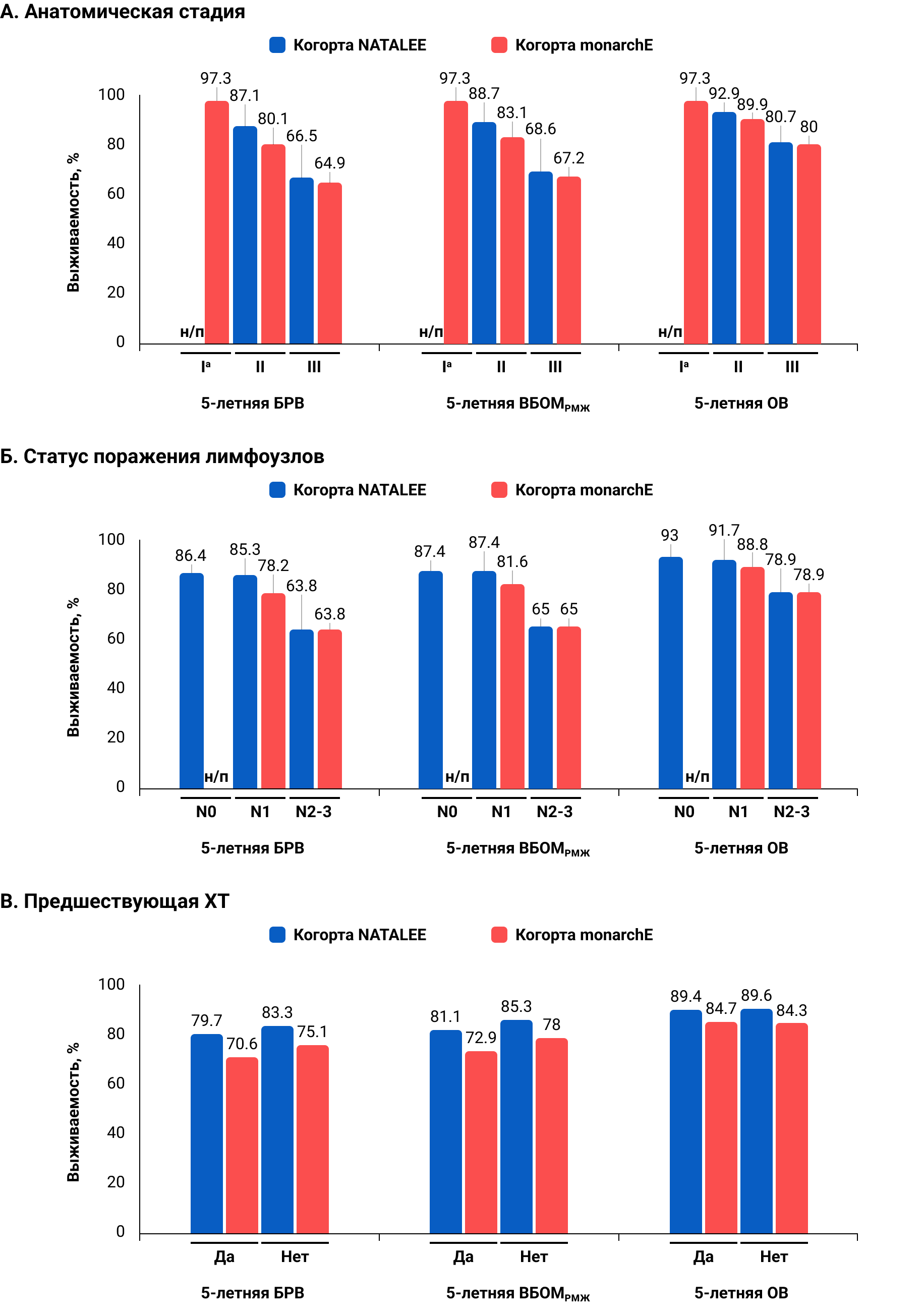
В обеих когортах БРВ, ВБОМРМЖ и ОВ снижались с увеличением стадии заболевания (рис. 3А). В когорте NATALEE показатели БРВ, ВБОМРМЖ и ОВ у пациентов с заболеванием N0 и N1 были аналогичны (рис. 3Б). В обеих популяциях пациенты, ранее не получавшие ХТ, имели немного лучшие показатели 5-летней БРВ и ВБОМРМЖ, чем пациенты, ранее получавшие ХТ (рис. 3В)14.
Рисунок 3. Подгрупповой анализ 5—летних рисков рецидива и смерти в зависимости от: А) стадии заболевания, Б) статуса поражения лимфоузлов, В) предшествующей ХТ14
a — Пациенты с заболеванием I стадии не соответствовали критериям NATALEE.
б — Пациенты с заболеванием N0 не соответствовали критериям monarchE.
Заключение
В когорте NATALEE пациенты с N0 имели такой же риск рецидива, как и пациенты с N1, что демонстрирует неудовлетворенную потребность в эффективной терапии для пациентов N0 с высоким риском рецидива14.
Несмотря на существующие современные стандарты лечения, как пациенты, соответствующие критериям NATALEE, так пациенты, соответствующие критериям monarchE, имели относительно высокую частоту отдаленных рецидивов в течение 5 лет (ВБОМРМЖ: 83,1% и 74,6% соответственно)14.
Несмотря на существующие современные стандарты лечения, как пациенты, соответствующие критериям NATALEE, так пациенты, соответствующие критериям monarchE, имели относительно высокую частоту отдаленных рецидивов в течение 5 лет (ВБОМРМЖ: 83,1% и 74,6% соответственно)14.
Результаты анализа, представленного на SABCS 2024, показывают значительный риск рецидива HR+ HER2− РМЖ, который в реальной клинической практике сохраняется у пациентов несмотря на применение современных подходов к адъювантной терапии, и подчеркивают необходимость разработки стратегий лечения, которые помогут снизить этот риск.
Определения
- БРВ — время от даты операции до первого инвазивного ипсилатерального рецидива РМЖ, инвазивного локорегионального рецидива, отдаленного рецидива или смерти по любой причине; БРВ не включает случаи инвазивного контралатерального РМЖ и событий второго первичного инвазивного рака (не РМЖ) (согласно STEEP 2.0).
- ВБОМРМЖ: время от даты операции до отдаленного рецидива или смерти по любой причине.
- ОВ: время от даты операции до смерти по любой причине.
Список сокращений
HR+ HER2− РМЖ — положительный по гормональным рецепторам и отрицательный по человеческому рецептору эпидермального фактора роста 2 типа рак молочной железы; G — гистологическая степень злокачественности; БРВ — безрецидивная выживаемость; ВБОМРМЖ — выживаемость без отдалённых метастазов РМЖ; ДИ — доверительный интервал; ИА — нестероидный ингибитор ароматазы; ОВ — общая выживаемость; ОР — отношение рисков; ЭТ — эндокринная терапия.
*NATALEE — открытое сравнительное исследование III фазы (n=5101), проводимое с целью оценки эффективности и переносимости комбинации рибоциклиба (400 мг в сутки, 21 день прием, 7 дней перерыв; продолжительность приема 3 года) и ИА (летрозол или анастрозол; продолжительность приема не менее 5 лет) по сравнению с монотерапией ИА. Первичная конечная точка (ВБИЗ) достигнута: 3-летняя ВБИЗ составила 90,7% vs 87,6% (ОР 0,749 (95%ДИ 0,628–0,892), p 0,0006) [HortobagyiG. et al. Ann Oncol. 2024:S0923–7534(24)04064–X]; 4-летняя ВБИЗ 88,5% vs 83,6% (ОР 0,715; 95%ДИ 0,69–0,84, p<0,0001) [Fasching P. et al. LBA13 — Ann Oncol. 2024;35 (suppl_2): 1–72].
**monarchE — открытое сравнительное исследование III фазы (n=5637), проводимое с целью оценки эффективности и переносимости комбинации абемациклиба + ЭТ по сравнению с моноЭТ. Первичная конечная точка достигнута: комбинация абемациклиб + ЭТ продемонстрировала статистически значимое улучшение ВБИЗ по сравнению с моноЭТ: ОР 0,680 (95% ДИ: 0,599–0,772); номинальный P < 0,001; медиана наблюдения 54 мес. [Johnston SRD, et al. J Clin Oncol. 2020;38(34):3987–3998; Rastogi P, et al. J Clin Oncol. 2024;42(9):987–993; Johnston SRD, et al. SABCS 2022. Oral GS1–09].
Препарат рибоциклиб не зарегистрирован в РФ для лечения раннего рака молочной железы. Данная информация носит научный характер в целях обмена научной информацией и не является способом продвижения фармацевтического продукта.
Список литературы
- Foldi J, et al. J Clin Oncol. 2019;37(16):1365-1369.
- Gomis RR, et al. Mol Oncol. 2017;11(1):62-78.
- Pedersen RN, et al. J Natl Cancer Inst. 2022;114(3):391-399.
- Pan H, et al. N Engl J Med. 2017;377(19):1836-1846.
- Slamon D, et al. N Engl J Med. 2024;390(12):1080-1091.
- Hortobagyi G, et al. SABCS 2023. Oral GS03-03.
- Fasching PA, et al. ESMO 2024. Oral LBA13.
- Johnston SRD, et al. J Clin Oncol. 2020;38(34):3987-3998.
- Rastogi P, et al. J Clin Oncol. 2024;42(9):987-993.
- Johnston SRD, et al. SABCS 2022. Oral GS1-09.
- Harbeck N, et al. Ann Oncol. 2021;32(12):1571-1581.
- Kisqali (ribociclib) [prescribing information]. East Hanover, NJ: Novartis Pharmaceuticals Corp; 2024.
- Verzenio (abemaciclib) [prescribing information]. Indianapolis, IN: Eli Lilly and Company; 2024.
- Tarantino P., et al. Risk of recurrence in real-world (RW) NATALEE- and monarchE-eligible populations of patients with HR+/HER2− early breast cancer (EBC) in an electronic health record (EHR)-derived database. SABCS, 2024, December 11. Poster presentation #P2-12-02.
1367385/RIB/web/02.25/0