Появление ингибиторов CDK4/6 для терапии HR+ HER2- рРМЖ позволило по-новому взглянуть на лечение пациенток. Прорывные данные по увеличению показателя общей выживаемости при лечении по схеме ЭТ + CDK4/6 привели к изменению взглядов на первую линию терапии.
Во всех обновленных клинических рекомендациях комбинация препаратов класса ингибиторов CDK4/6 в сочетании с ЭТ является предпочтительной схемой лечения HR+ HER2- рРМЖ: Клинические рекомендации МЗ 2020, RUSSCO, РООМ, NCCN, ESMO1-5.
В клинических исследованиях MONALEESA, PALOMA и MONARCH продемонстрированы результаты лечения HR+ HER2- РМЖ в пре-, пери- и постменопаузе по сравнению с группой плацебо + ЭТ. Отсутствие прямых сравнительных исследований между препаратами вызывает затруднения в сравнении эффективности и безопасности схем с их использованием. Вопрос о наиболее предпочтительной схеме среди ингибиторов CDK4/6 до сих пор открыт.
Цель данного обзора — рассмотреть результаты сравнительных анализов и проанализировать данные, продемонстрированные в клинических исследованиях.
Особенности и различия ингибиторов CDK4/6
На данный момент доступны 3 разных ингибитора CDK4/6, но они по многим факторам имеют отличия6,7,8.
-
Разная молекулярная структура
-
Разные фармакокинетические параметры
-
Разная активность в отношении CDK4 и CDK6
-
Разный уровень свободного препарата в тканях
-
Разная клиническая эффективность
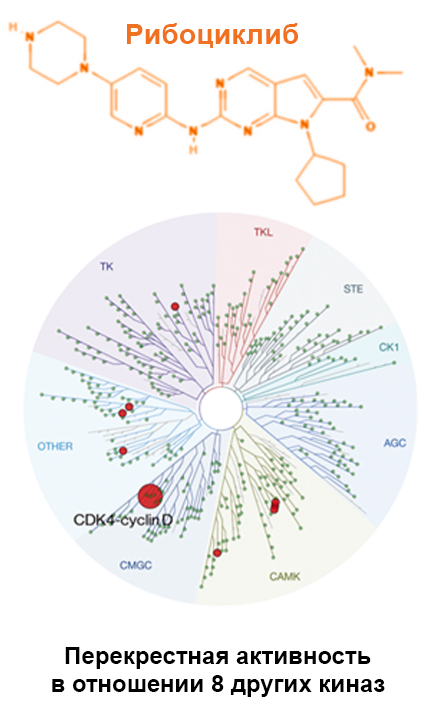
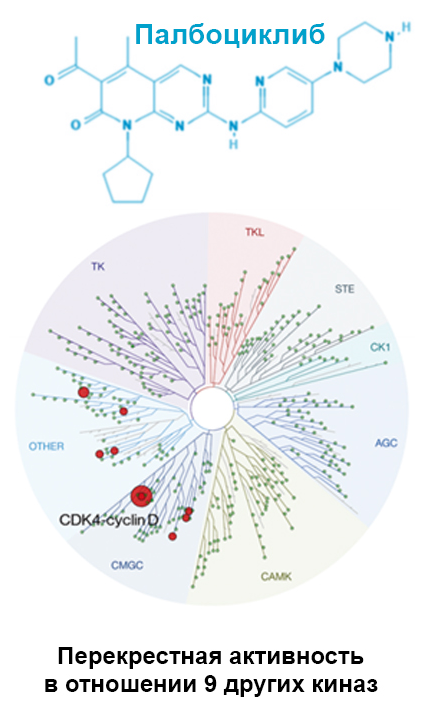
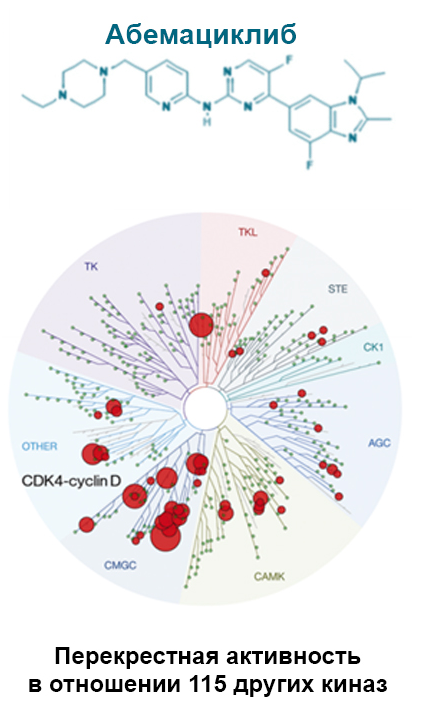
Молекулярные различия в структуре ингибиторов CDK4/6 косвенно влияют на результаты применения при рРМЖ.
Эффективность ингибиторов CDK4/6 при распространенном РМЖ
Общая выживаемость
Данные, полученные в ходе исследований, демонстрируют преимущество применения ингибиторов CDK4/6 в первой линии терапии метастатического РМЖ — только эти препараты впервые доказали увеличение общей выживаемости совместно с ЭТ. Подобные комбинации ингибитора CDK4/6 с гормонотерапией должны стать новым стандартом в лечении рРМЖ1.
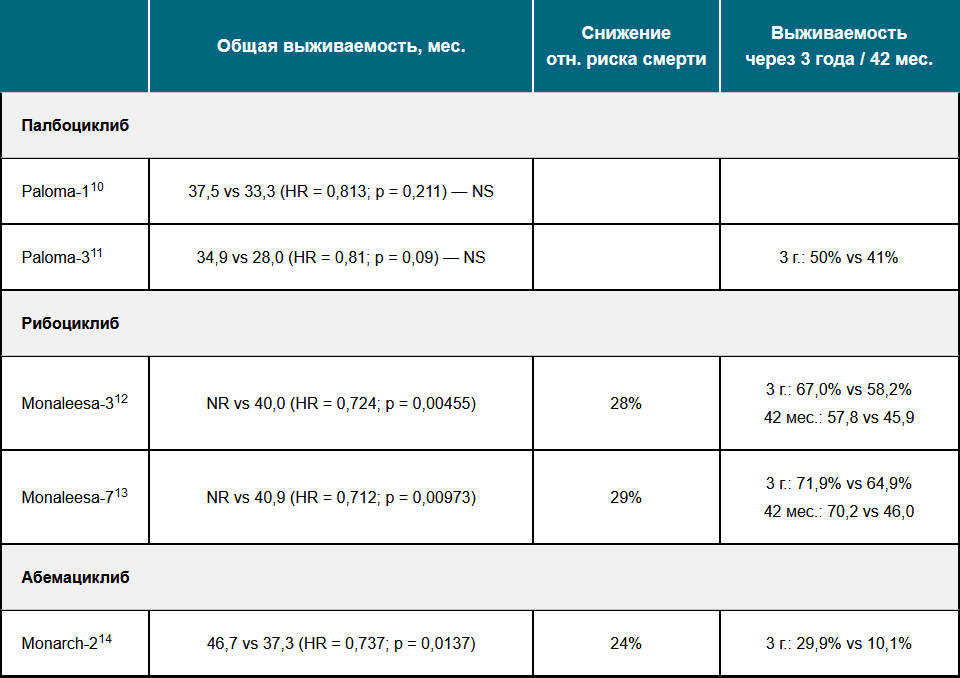
Примечание.
NR — не достигнут; NS — нет статистически значимых отличий.
Рибоциклиб — единственный ингибитор CDK4/6, дважды доказавший статистически значимое увеличение ОВ15,16.
Выживаемость без прогрессии
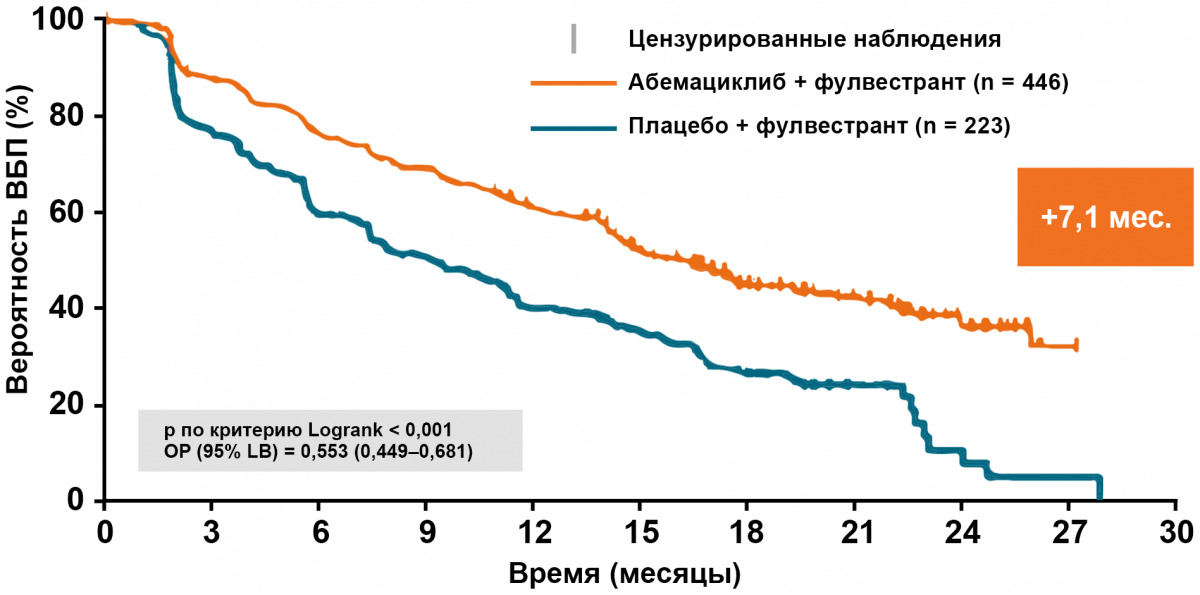
В ходе исследований MONALEESA (рибоциклиб), PALOMA (палбоциклиб) и MONARCH (абемациклиб) удалось получить увеличение выживаемости без прогрессирования практически в 2 раза у женщин с HR+ HER2- метастатическим РМЖ.
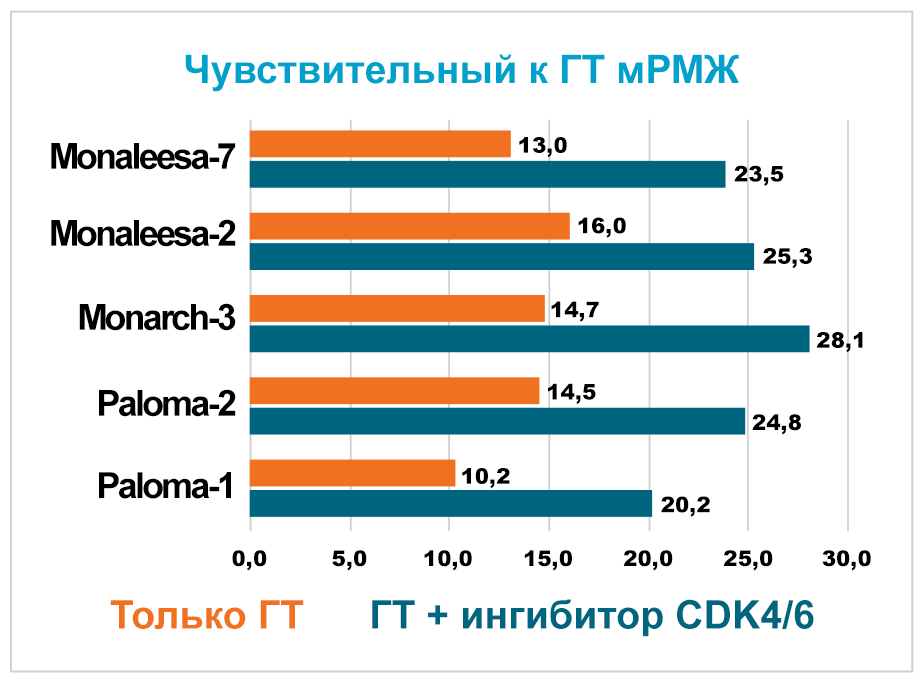
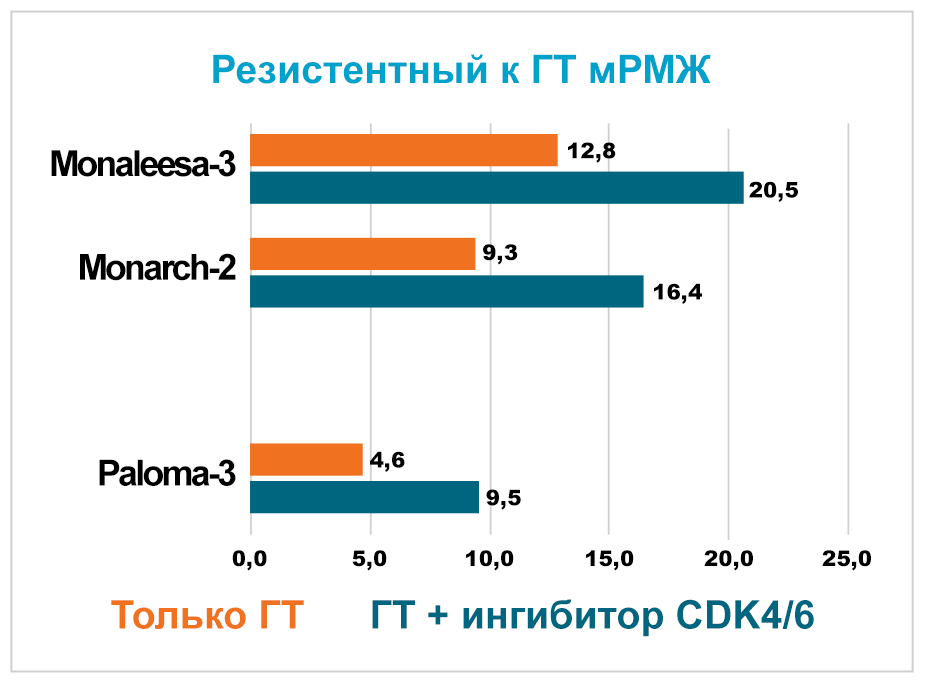
* Адаптировано из Marra A. and Curigliano G. NPJ Breast Cancer (2019)
Серия исследований MONALEESA доказывают, что применение рибоциклиба позволяет увеличить выживаемость без прогрессирования в 1,5–2 раза у женщин с HR+ HER2- метастатическим РМЖ. Эффективность и безопасность рибоциклиба изучены в трех клинических исследованиях III фазы.
MONALEESA-2: пациентки в постменопаузе, 1 линия + летрозол18
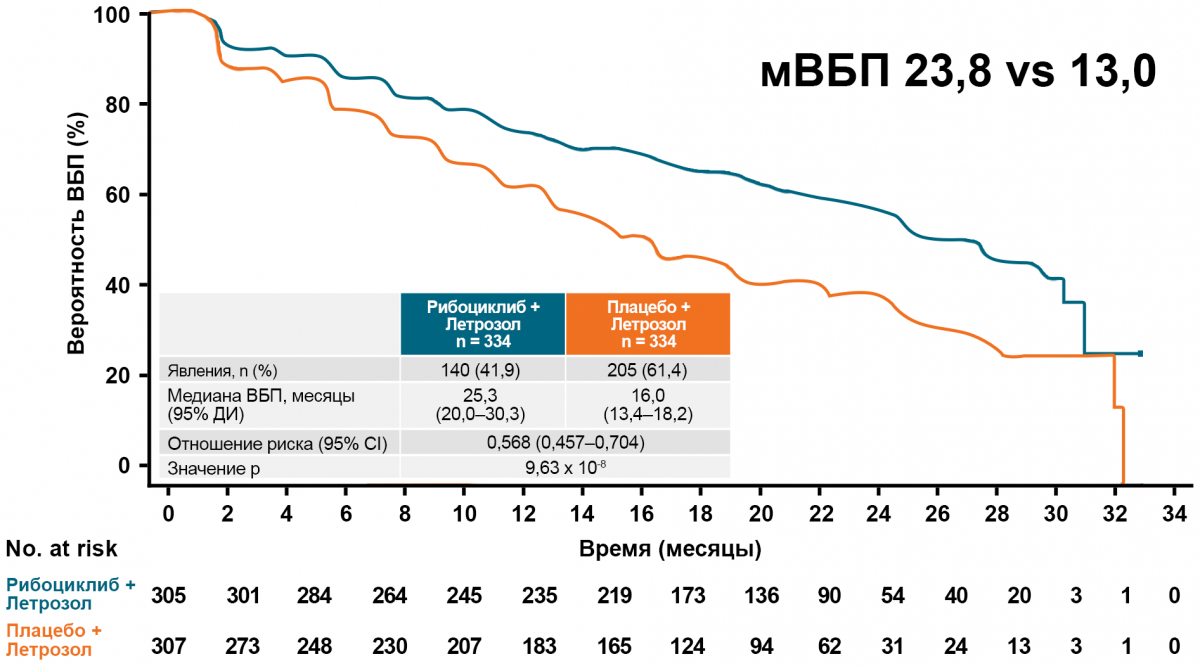
MONALEESA-3: пациентки в постменопаузе, 1 и 2 линии + фулвестрант19
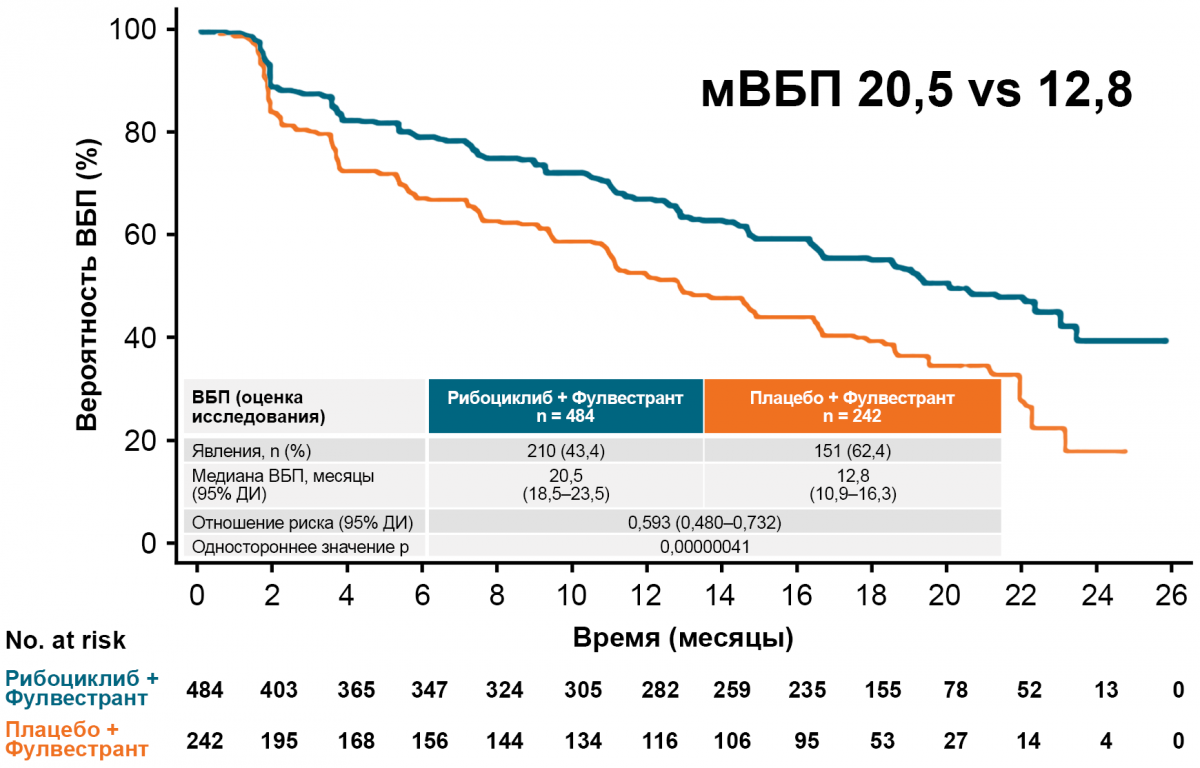
MONALEESA-7: выживаемость без прогрессирования
Примечание.
* ВБП — выживаемость без прогрессирования; ИА — ингибиторы ароматазы; ОР — отношение рисков; ДИ — доверительный интервал.
Tripathy D. et al. Lancet Oncol. 2018;19(7):904–915
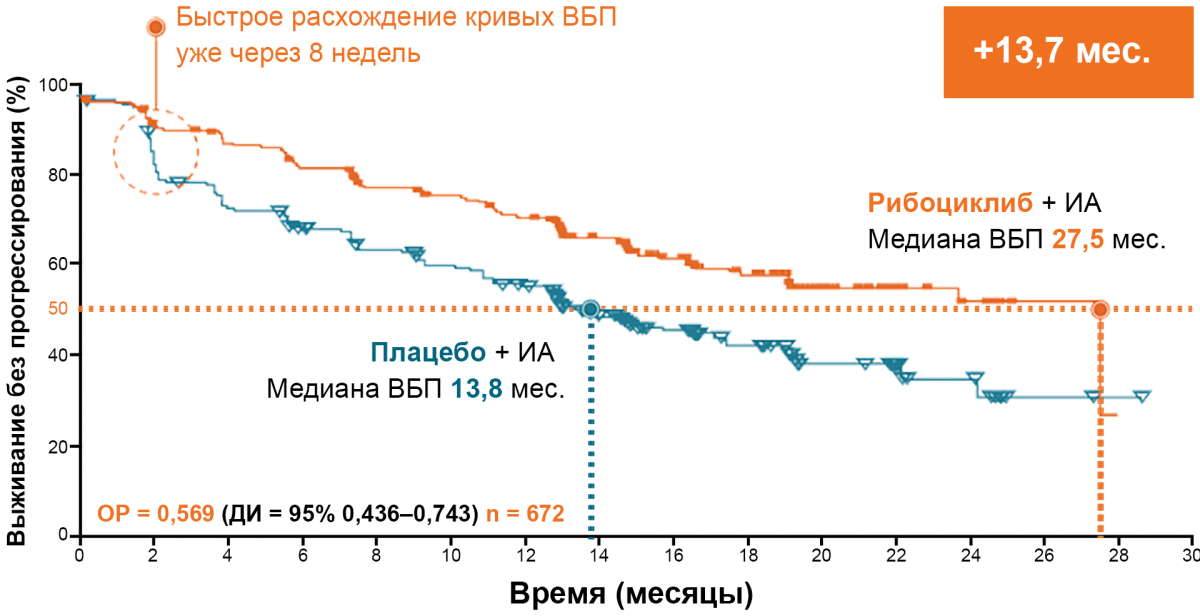
MONALEESA-7: пациентки в пре- и перименопаузе, без предшествующей гормонотерапии + НСИА20
Практическое применение инновационных препаратов стало более доступным после включения рибоциклиба в перечень ЖНВЛП30.
Во все исследования MONALEESA были включены пациентки, представляющие особый интерес — более половины больных в каждом из исследований имели метастазы в различные органы: легкие, печень и головной мозг. Подгрупповой анализ всех трех исследований показал, что добавление ингибиторов CDK4/6 к ЭТ значительно увеличивает общую выживаемость и выживаемость без прогрессии.
Применение ингибиторов CDK4/6 и ингибиторов ароматазы в первой линии гормонотерапии
Сравнение общей выживаемости без прогрессирования21,22,23.
Paloma-2: выживаемость без прогрессирования
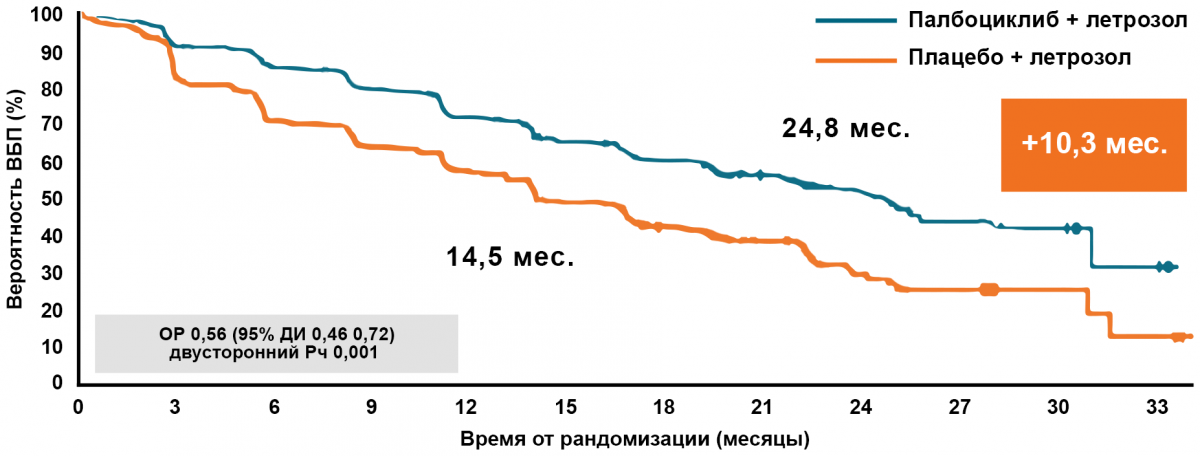
Monaleesa-2: выживаемость без прогрессирования
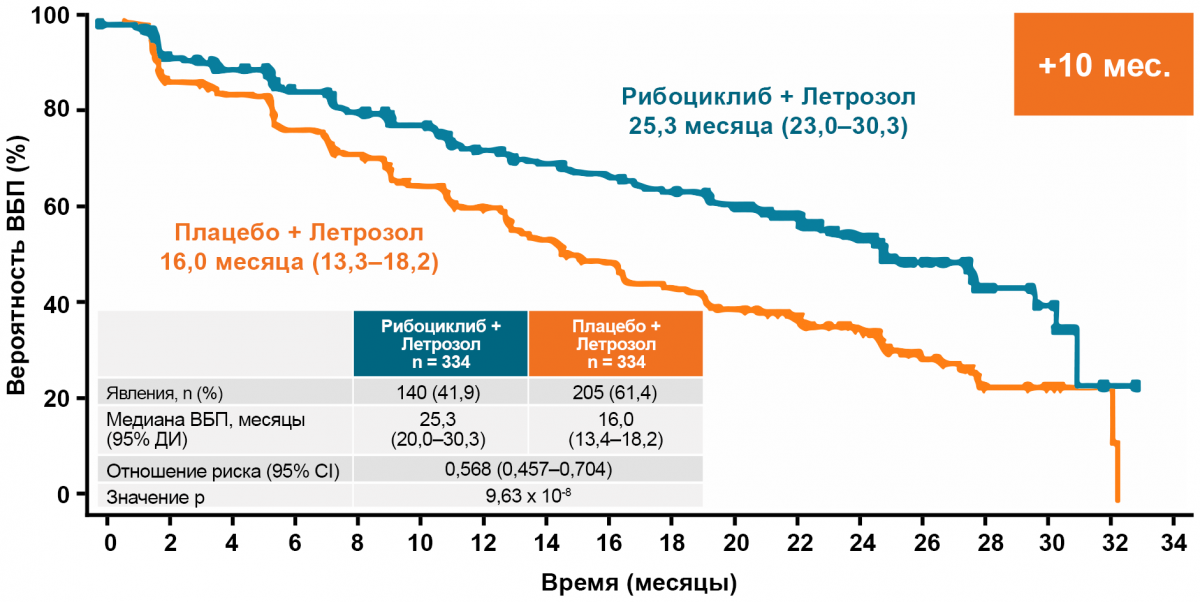
Monarch-3: выживаемость без прогрессирования
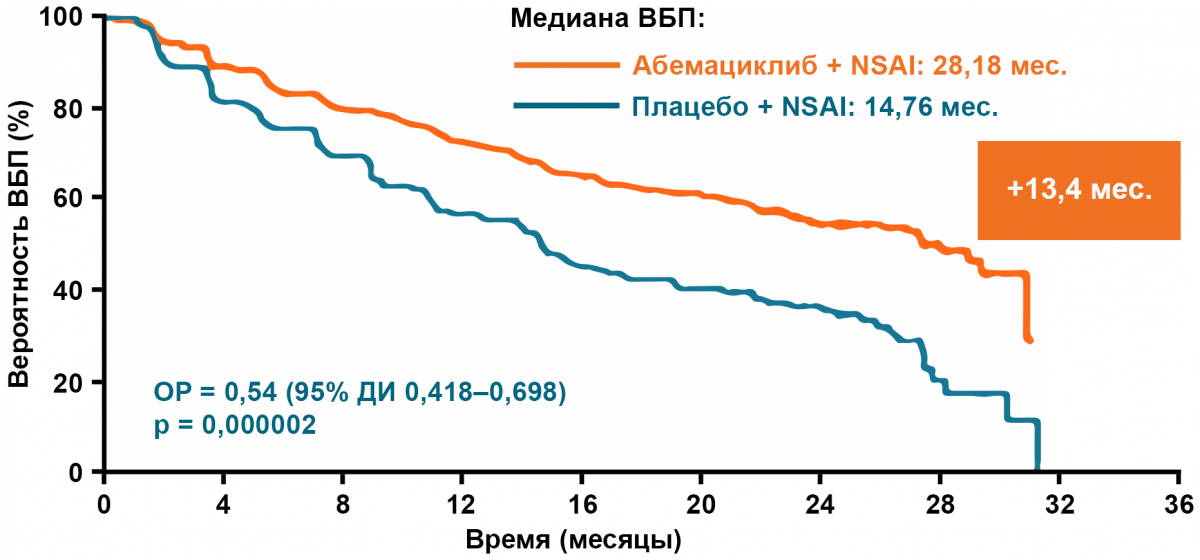
Применение ингибиторов CDK4/6 и фулвестранта во второй линии гормонотерапии
Сравнение общей выживаемости без прогрессирования24,25,26.
Paloma-2: выживаемость без прогрессирования
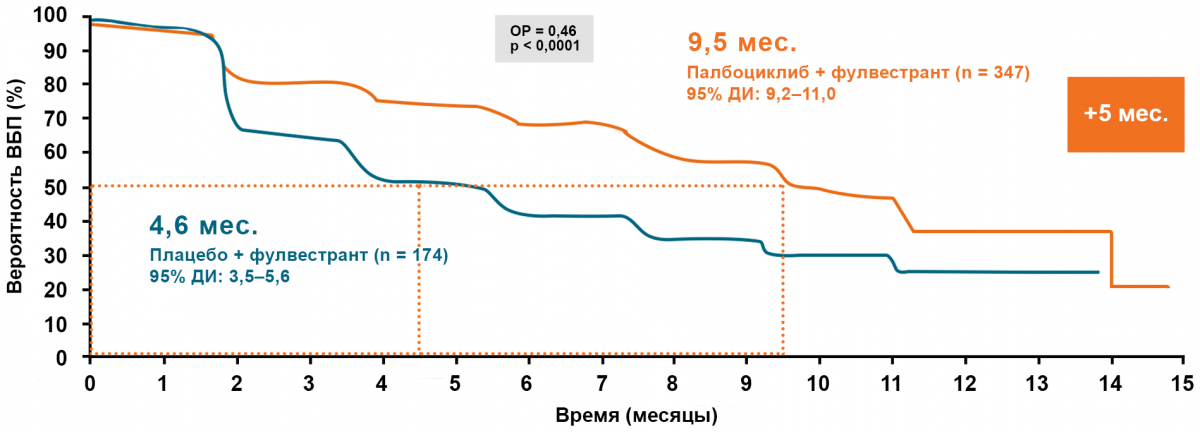
Monaleesa-3: выживаемость без прогрессирования
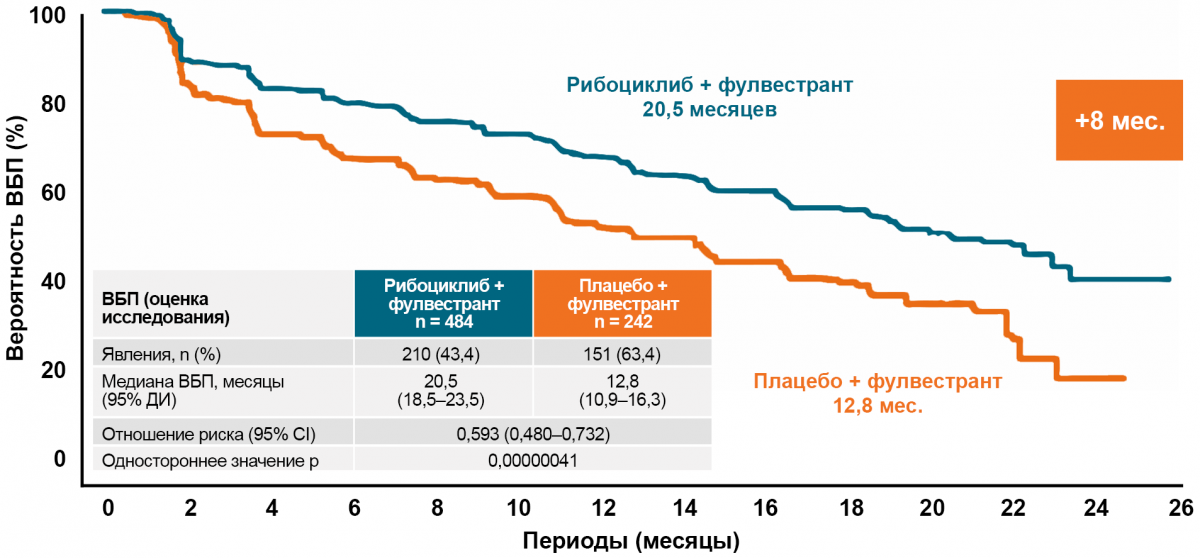
Безопасность
Одним из убедительных аргументов для использования ингибиторов CDK4/6 в клинической практике является доказанная безопасность — большинство пациентов хорошо переносят прием этих препаратов в ежедневном режиме. Ингибиторы циклин-зависимых киназ хоть и имеют схожий спектр токсичности, но отличаются по выраженности и некоторым видам нежелательных явлений.
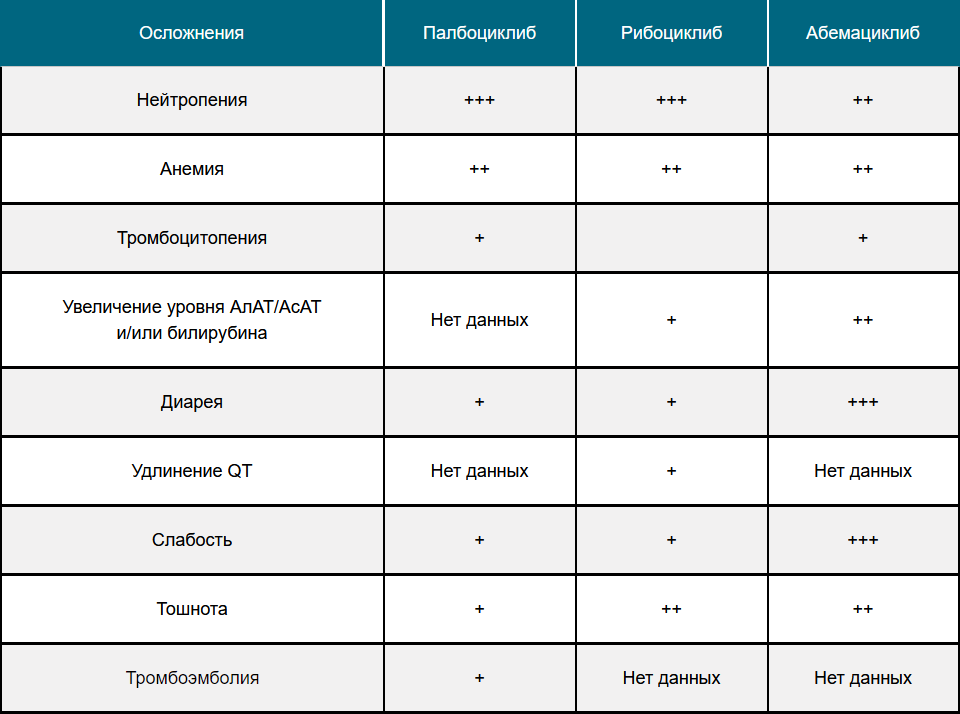
Практически все побочные эффекты, связанные с ингибиторами CDK4/6, предсказуемы и быстро обратимы после приостановки терапии или редукции дозы препаратов. Исследования показывают, что незначительные различия могут быть связаны с разной избирательностью воздействия на ферменты CDK4 и CDK627,28,29.
Литература:
- Клинические рекомендации. Рак молочной железы 2020. Электронный ресурс: http://cr.rosminzdrav.ru/#!/recomend/236 Дата обращения: 16.04.2020.
- Стенина М.Б. и соавт. RUSSCO #3s2, 2019 (том 9). С. 128–163.Электронный ресурс https://rosoncoweb.ru/standarts/RUSSCO/2019/2019-08.pdf Дата обращения: 16.04.2020.
- Клинические рекомендации РООМ по лечению метатического рака молочной железы.
- National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology: Breast Cancer. V.3.2020 Электронный ресурс: https://www.nccn.org/professionals/physician_gls/pdf/breast.pdf Дата обращения 16.04.2020.
- Cardoso et al. Annals of Oncology. 2018. 29: 1634–1657. Электронный ресурс: https://www.sciencedirect.com/science/article/pii/S0923753419341134?via%3Dihub Дата обращения 16.04.2020.
- Marra A. and Curigliano G. NPJ Breast Cancer (2019) 5:27.
- Kim S. et al. Oncotarget. 2018;9(81):35226-35240.
- Chen P. et al. Mol Cancer Ther. 2016;15(10):2273-2281.
- Landmark Studies Show Clear Overall Survival Benefit for CDK4/6 Inhibitors in Advanced Breast Cancer, https://ascopost.com/issues/october-25-2019/cdk46-inhibitors-in-advanced-breast-cancer/
- Finn et al. J Clinical Oncology 2017 35:15_suppl, 1001-1001.
- Turner et al. N Engl J Med 2018; 379:1926-1936.
- Slamon et al. N Engl J Med 2020; 382:514-524.
- Im et al. N Engl J Med 2019;381:307-16.
- Sledge et al. JAMA Oncol. 2020;6(1):116-124.
- Slamon D. et al. J Clin Oncol. 2018;36(24):2465-2472.
- Tripathy D. et al. Lancet Oncol. 2018;19(7):904-915.
- Кононенко И.Б. и др. Медицинский совет. 2019; 10: 42-55.
- Hortobagyi et al. Annals of Oncology0: 1–7, 2018.
- Tripathy et al. Lancet Oncol 2018; 19: 904–15.
- Clin Oncol 36, 2018.
- Finn R.S. et al. N Engl J Med 2016;7;375(20):1925–1936.
- Goetz M.P. et al. Presented at AACR 2018.
- Hortobagyi G.N. et al. ASCO 2017, Poster 1038.
- Turner N.C. et al. SABCS 2016 (Abstract P4-22-06).
- Slamon D.J. ASCO 2018.
- Sledge G.W. et al. J Clin Oncol 2017.
- Marc Thill and Marcus Schmidt Management of adverse events during cyclin-dependent kinase 4/6 (CDK4/6) inhibitor-based treatment in breast cancer. Ther Adv Med Oncol. 2018;10:1–12.
- Кононенко И.Б., Снеговой А.В. и др. Протокол коррекции осложнений, возникающих при лечении ингибиторами CDK4/6. Протоколы клинических рекомендаций поддерживающей терапии в онкологии. 2018:196-205. [Kononenko I.B., Snegovoi A.V. et al. Protocol for management of complications of CDK4/6 inhibitors therapy. Protocols of clinical guidelines for maintenance therapy in oncology. 2018:196-205] (In Russ).
- Gelbert L.M., Cai S., Lin X. et al. Preclinical characterization of the CDK4/6 inhibitor LY2835219: in-vivo cell cycle-dependent/independent antitumor activities alone/in combination with gemcitabine. Invest New Drugs. 2014;32:825-837.
- Распоряжение Правительства РФ от 12.10.2019 N 2406-р.
11247202/RIB/web/08.24/0