Оглавление
- Предпосылки применения тройной комбинации (BRAFi + MEKi + анти-PD-L1)в лечении меланомы кожи
- Сравнение эффективности двойной и тройной комбинаций
- Сравнение переносимости двойной и тройной комбинаций
- Ключевые выводы
Предпосылки применения тройной комбинации (BRAFi + MEKi + анти-PD-L1) в лечении меланомы кожи
В настоящее время в клинической практике применяют две основные стратегии лечения метастатической меланомы кожи – таргетную терапию (ТТ) и иммуноонкологическую терапию (ИТ)1. Эти методы реализуют свое действие с помощью разных механизмов, но оба показывают высокую эффективность при применении у пациентов.1, 2, 3
Предпосылками для сочетанного применения ТТ и ИТ при меланоме кожи послужили следующие данные :
- ТТ при меланоме кожи обеспечивает высокую частоту, но меньшую продолжительность объективного ответа. ИТ, наоборот, демонстрирует меньшую частоту при более высокой продолжительности объективного ответа2. Можно предположить, что сочетание ТТ и ИТ положительно скажется на частоте и длительности объективного ответа, а это повлияет на выживаемость пациентов с меланомой кожи2.
- В течение 2 недель после начала ТТ BRAFi повышается уровень PD-1 и его лиганда PD-L1, что может являться основой механизма развития резистентности меланомы кожи к данному виду терапии. Добавление анти-PD-L1 препарата к ТТ предположительно может снизить вероятность развития этой резистентности и продлить ответ на ТТ2.
Около 10 лет назад были начаты первые клинические исследования в отношение сочетанного применения ТТ и ИТ при лечении пациентов с меланомой кожи2.
Появление новой опции в лечении метастатической меланомы кожи – сочетанной ТТ+ИТ в виде тройной комбинации BRAFi + MEKi + анти-PD-L1 – поставило перед практикующим врачом ряд вопросов, на которые следует ответить перед принятием решения о выборе способа терапии:
- Повышается ли эффективность лечения при добавлении анти-PD-L1 к комбинации BRAFi + MEKi?
- Изменяется ли переносимость лечения при добавлении анти-PD-L1 к комбинации BRAFi + MEKi?
- Cмогли ли клинические исследования подтвердить фундаментальные предпосылки применения триплета?
- Какая терапия может быть назначена после тройной комбинации?

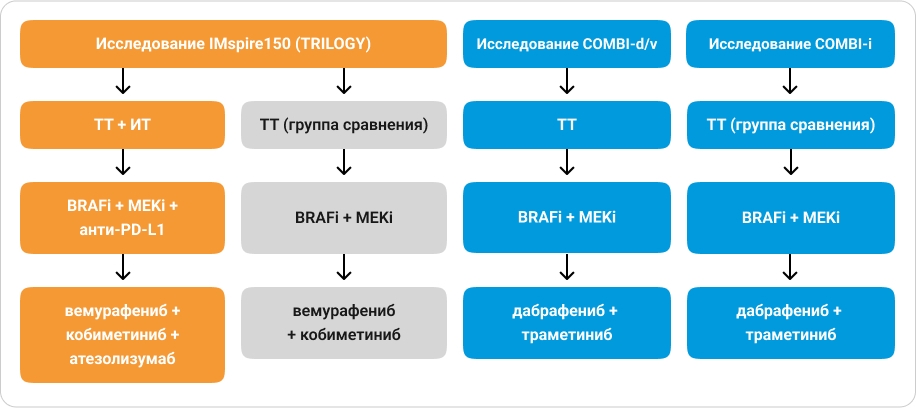
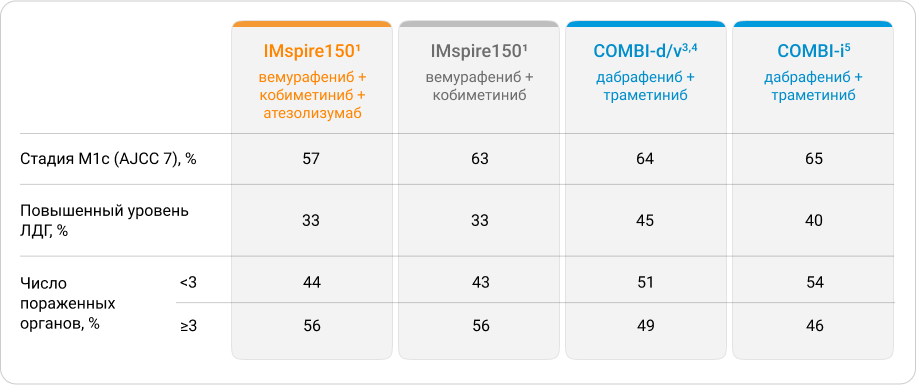
Для ответа на данные вопросы можно сравнить полученные в исследовании IMspire150 (TRILOGY) результаты оценки эффективности и переносимости тройной комбинации BRAFi + MEKi + анти-PD-L1 с результатами лечения пациентов с метастатической меланомой кожи двойной комбинацией BRAFi + MEKi согласно данным различных исследований (IMspire150, COMBI-d/v, COMBI-i). В исследованиях IMspire150, COMBI-d/v и COMBI-i популяции пациентов были сопоставимы по уровню ЛДГ, числу зон, пораженных метастазами, и по числу пациентов с висцеральными метастазами. Кроме того, ни в одно из исследований не были включены пациенты с метастазами в головной мозг. Это позволяет проводить непрямое сравнение результатов данных исследований.
Таблица 1 – Характеристика пациентов с метастатической меланомой кожи, участвовавших в исследованиях двойной и тройной комбинаций
Стоит отметить, что в исследовании IMspire150 был использован модифицированный дизайн приема препаратов. Во-первых, он был разделен на несколько циклов, первый месяц пациенты получали только двойную таргетную терапию, во-вторых, при использовании тройной комбинации, дозировка вемурафениба была снижена на 25% по причине высокой токсичности триплета1.
Подробнее об исследовании COMBI-d/v можно прочитать здесь.
Подробнее об исследовании COMBI-i можно прочитать здесь.
Сравнение эффективности двойной и тройной комбинации
Влияние на выживаемость без прогрессирования
Применение тройной комбинации привело к увеличению медианы ВБП до 15,1 месяца у пациентов, принимающих вемурафениб + кобиметиниб + атезолизумаб, по сравнению с 10,6 месяца для двойной комбинации вемурафениб + кобиметиниб и 11,1-12 месяцами для двойной комбинации дабрафениб + траметиниб1, 3, 5. С увеличением длительности наблюдения можно отметить нарастание различий в показателях ВБП после приема тройной комбинации по сравнению с двойной. Так, через 6 месяцев наблюдения различия между показателями минимальны – 73% против 74%, а через 12 месяцев – 54% против 45% в исследовании IMspire150, и 50% для комбинации дабрафениба и траметиниба в исследовании COMBI-i1, 5.
Полученные результаты указывают на возможный отсроченный эффект сочетанной терапии, однако окончательные выводы можно будет делать только после завершения предусмотренного срока наблюдения за пациентами и итогового анализа результатов.
Влияние на общую выживаемость
Второй промежуточный анализ результатов в исследовании IMspire150 показал численно более длительную ОВ в группе триплета (медиана 39,0 месяцев) по сравнению с двойной комбинацией (25,8 месяцев). Однако разница между этими показателями была статистически не значима (р=0,14)6.
Кроме того, согласно последним данным исследования COMBI-i, в группе пациентов, получавших дабрафениб + траметиниб, медиана ОВ составила 40,4 месяца, что выше медианы ОВ в группе тройной комбинации 39,0 месяцев. По показателю 2-летней ОВ нет разницы между тройной комбинацией и двойной комбинацией дабрафениб + траметиниб: 62% против 62%6, 7.
Предполагалось, что добавление атезолизумаба к ТТ увеличит продолжительность ответа, однако тройная комбинация не показала преимущества по данному показателю в сравнении с результатами дабрафениба и траметиниба, медиана длительности ответа составила 21 месяц для тройной комбинации и 20,7 месяца для комбинации дабрафениб + траметиниб6, 7.
Таблица 2 – Показатели общей выживаемости двойной и тройной комбинации
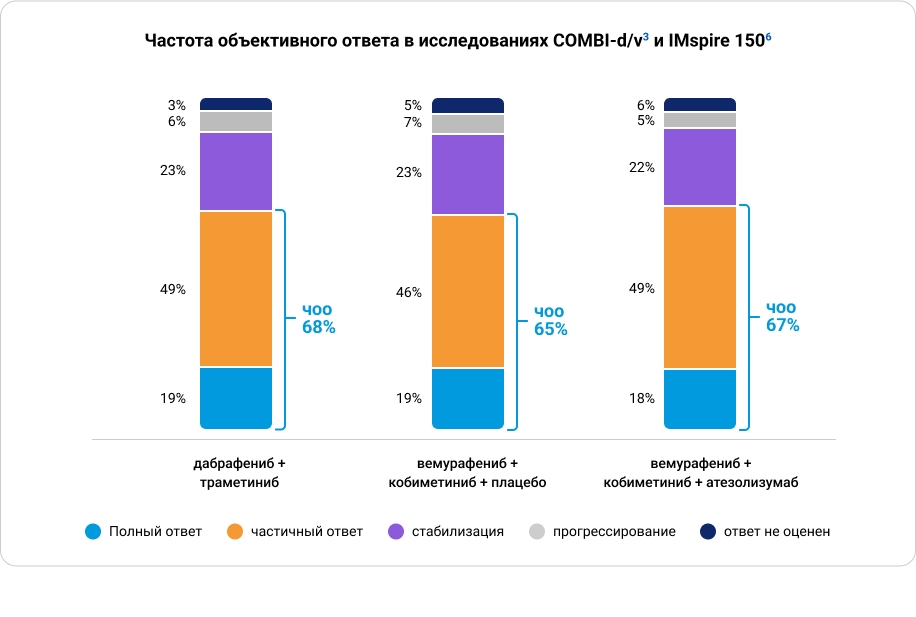
Влияние на частоту объективного ответа опухоли на лечение
Показатель ЧОО метастатической меланомы на терапии триплетом вемурафениб + кобиметиниб + атезолизумаб сопоставим с аналогичными показателями, полученными при лечении пациентов только ТТ, как комбинацией вемурафениб + кобиметиниб, так и комбинацией дабрафениб + траметиниб3, 6.
Сравнение переносимости двойной и тройной комбинации
Добавление к схеме ТТ метастатической меланомы кожи ингибитора контрольных точек анти-PD-L1 может повысить токсичность применяемой схемы терапии, в том числе за счет появления иммуноопосредованных нежелательных явлений (НЯ)1.
Таблица 3 – Показатели переносимости двойной и тройной комбинаций:
В исследовании IMspire150 в группе вемурафениб + кобиметиниб + атезолизумаб частота НЯ ≥3 степени тяжести была выше более чем в 2 раза по сравнению с двойной комбинацией дабрафениб + траметиниб в исследовании COMBI-i. Отмена терапии из-за НЯ также встречалась в 1,5 раза чаще в группе тройной комбинации, чем на терапии дабрафениб + траметиниб. Кроме того, более чем половине пациентов потребовалось назначение глюкокортикостероидов из-за развития иоНЯ1, 5, 6.
По мнению исследователей, два нежелательных явления 5 степени (молниеносный гепатит и печеночная недостаточность) в исследовании IMspire150 в группе вемурафениб + кобиметиниб + атезолизумаб были связаны именно с применением триплета1.
Ключевые выводы
- Триплет вемурафениб + кобиметиниб + атезолизумаб в исследовании IMspire150 незначительно увеличивал продолжительность ВБП, однако не показал статистически значимого увеличения ОВ и ЧОО по сравнению с двойной комбинацией вемурафениб + кобиметиниб.
- По данным непрямого сравнения двойная комбинация дабрафениб + траметиниб не уступает триплету вемурафениб + кобиметиниб + атезолизумаб по показателям ЧОО, ОВ и длительности ответа.
- Двойная комбинация дабрафениб + траметиниб имеет более благоприятный профиль безопасности по сравнению с триплетом вемурафениб + кобиметиниб + атезолизумаб.
- Вопрос о последующей линии терапии после применения триплета, включающего уже и таргетную, и иммуноонкологическую терапию, пока остается открытым?

Список сокращений
- ВБП – выживаемость без прогрессирования
- ИТ – иммунная терапия
- ЛДГ – лактатдегидрогеназа
- НЯ – нежелательные явления
- иоНЯ - иммуноопосредованные нежелательные явления
- ОВ – общая выживаемость
- ТТ – таргетная терапия
- BRAFi – ингибиторы BRAF
- MEKi – ингибиторы MEK
Литература:
- Gutzmer R. et al. Atezolizumab, vemurafenib, and cobimetinib as first-line treatment for unresectable advanced BRAFV600 mutation-positive melanoma (IMspire150): primary analysis of the randomised, double-blind, placebo-controlled, phase 3 trial //The Lancet. – 2020. – Т. 395. – №. 10240. – С. 1835-1844
- Wargo J. A., Cooper Z. A., Flaherty K. T. Universes collide: combining immunotherapy with targeted therapy for cancer // Cancer discovery. – 2014. – Т. 4. – №. 12. – С. 1377-1386.
- Robert C. et al. Five-year outcomes with dabrafenib plus trametinib in metastatic melanoma // New England Journal of Medicine. – 2019. – Т. 381. – №. 7. – С. 626-636.
- Long G. V. et al. Factors predictive of response, disease progression, and overall survival after dabrafenib and trametinib combination treatment: a pooled analysis of individual patient data from randomised trials //The lancet oncology. – 2016. – Т. 17. – №. 12. – С. 1743-1754.
- Dummer R. et al. Randomized phase III trial evaluating spartalizumab plus dabrafenib and trametinib for BRAF V600–mutant unresectable or metastatic melanoma //Journal of Clinical Oncology. – 2022. – Т. 40. – №. 13. – С. 1428.
- Ascierto P. A. et al. Overall survival with first-line atezolizumab in combination with vemurafenib and cobimetinib in BRAFV600 mutation-positive advanced melanoma (IMspire150): second interim analysis of a multicentre, randomised, phase 3 study //The Lancet Oncology. – 2023. – Т. 24. – №. 1. – С. 33-44.
- Dummer R. et al. Dabrafenib (D) and trametinib (T) plus spartalizumab (S) in patients (pts) with previously untreated BRAF V600–mutant unresectable or metastatic melanoma: Three-year overall survival (OS) data from the randomized part 3 of the phase III COMBI-i trial. – ASCO 2022. – 2022. - S. 16. - 9527.
11310322/ONCO/DIG/11.24/0