Почему нам интересны данные реальной клинической практики?
Опыт пострегистрационного применения лекарственных препаратов показывает, что не всегда данные реальной клинической практики (РКП) совпадают с показателями эффективности и безопасности, полученными при проведении регистрационных рандомизированных клинических исследований (РКИ)1, 2, 3. Результаты применения препарата в реальных условиях представляют большой интерес для практикующих врачей. Чем это обусловлено?
- Популяция пациентов в реальных условиях шире, чем когорта пациентов, отобранных для участия в РКИ. Критерии отбора пациентов для РКИ обычно очень жесткие. После регистрации лекарственный препарат получают пациенты, которые могут отличаться по возрасту, спектру сопутствующих заболеваний, общему состоянию и другим характеристикам от пациентов, которые участвовали в РКИ. Как следствие, показатели эффективности применения препарата в такой расширенной популяции могут отличаться от соответствующих показателей при проведении РКИ. При этом данные РКП являются более репрезентативными для реальной популяции пациентов, чем результаты РКИ1, 2, 3.
- В условиях РКП могут быть выявлены редкие или отсроченные нежелательные явления (НЯ). РКИ часто проводят с участием небольшой (по сравнению с масштабами реального применения) когорты пациентов в условиях ограниченного времени наблюдения. В связи с этим РКИ не всегда дают возможность выявить редкие или отсроченные НЯ, которые могут быть обнаружены при применении лекарственного препарата в условиях РКП1.
- В условиях РКП можно оценить эффективность и безопасность схем лечения, не изученных напрямую при проведении РКИ, например, последовательного применения нескольких вариантов терапии.
- При проведении адъювантной терапии у пациентов с меланомой кожи в условиях РКП можно получить более точную информацию об эффективности терапии при разных подстадиях меланомы. Особенно это актуально в связи с изменением подхода к стадированию меланомы в 2017 году, когда РКИ адъювантной терапии у пациентов с меланомой кожи уже были начаты.
В последние годы были опубликованы результаты нескольких крупных исследований РКП, направленных на оценку эффективности адъювантной таргетной терапии комбинацией дабрафениб + траметиниб (комбoТТ) и иммуноонкологической терапии анти-PD-1 препаратами (моноИТ) у пациентов после удаления меланомы кожи.
Обсудим результаты этих исследований и ответим на два вопроса:
- Как соотносятся данные РКИ и РКП?
- Сохраняется ли преимущество комбoТТ перед моноИТ в реальных условиях?
Исследование РКП J. Placzke и соавт. (Польша, 2023)
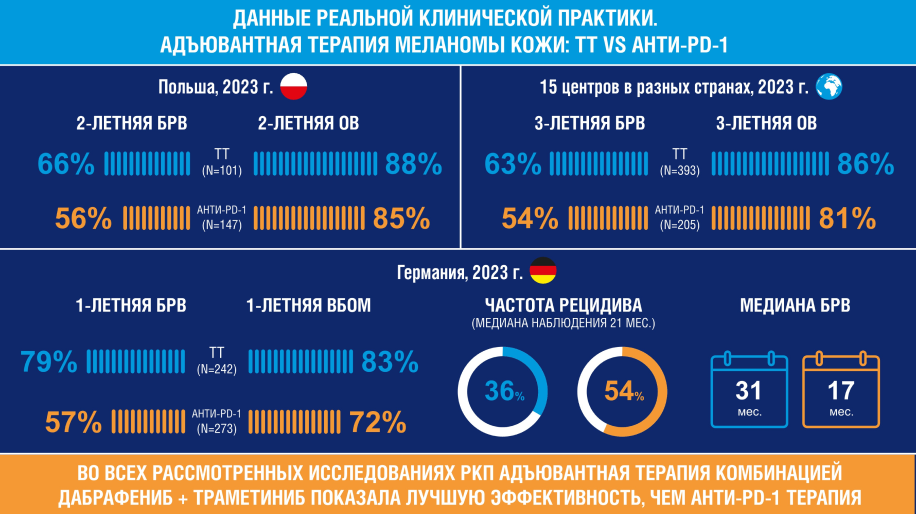
В 2023 году польскими исследователями был выполнен анализ эффективности и безопасности адъювантной терапии у 248 пациентов с III—IV стадиями меланомы кожи согласно AJCC 8 в условиях РКП. Из них 147 пациентов получали адъювантную терапию анти-PD-1 препаратами (моноИТ: 56% ниволумаб, 44% пембролизумаб), 101 пациент — адъювантную комбинированную таргетную терапию (комбоТТ: дабрафениб + траметиниб)1. Пациенты, получавшие адъювантную терапию в реальных условиях, по ряду характеристик отличались от пациентов, отобранных по жестким критериям для участия в РКИ ниволумаба, пембролизумаба и комбинации дабрафениб + траметиниб (табл. 1).
Таблица 1. Различия в характеристиках пациентов в исследовании РКП J. Placzke и соавт. (Польша, 2023)1 и РКИ Keynote-0544, COMBI-AD5 и CheckMate-2386.
Изменилась ли эффективность адъювантной терапии при ее проведении у расширенной популяции пациентов в реальных условиях? Посмотрим на данные в таблице 2 и сравним основные показатели эффективности адъювантной терапии в исследовании J. Placzke (РКП) и в соответствующих РКИ.
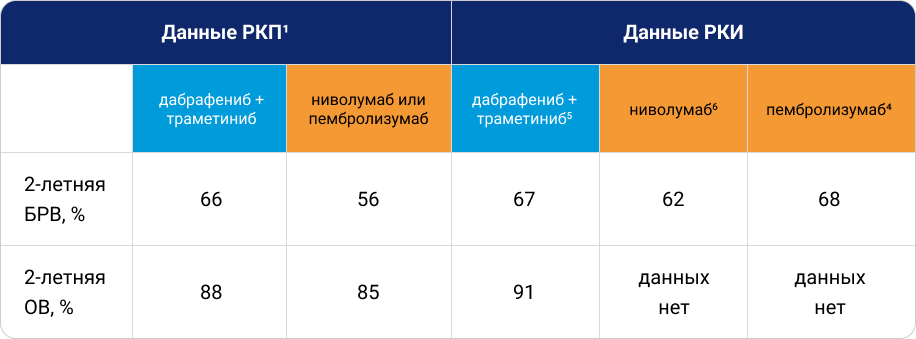
Таблица 2. Эффективность адъювантной комбоТТ и моноИТ после резекции меланомы кожи: данные РКП в исследовании J. Placzke и соавт. (Польша, 2023)1 и РКИ Keynote-0544, CheckMate-2386 и COMBI-AD5.
В реальных условиях эффективность адъювантной моноИТ по показателю 2-летней БРВ оказалась несколько ниже: 56,1% по сравнению с 62—68% согласно данным РКИ1, 4, 6. При этом 2-летняя БРВ для комбинации дабрафениб + траметиниб практически не изменилась: 65,9% против 67% в РКИ1, 5. Соответственно, сохранилось преимущество комбоТТ по сравнению с моноИТ, разница составила почти 10%1.
Связь между развитием НЯ, связанных с лечением (НЯсл), и БРВ
Авторами были получены интересные данные, демонстрирующие связь между развитием НЯсл и частотой рецидивирования меланомы кожи в группе адъювантной моноИТ (табл. 3).
Таблица 3. Безрецидивная выживаемость на фоне адъювантной моноИТ после резекции меланомы кожи у пациентов с НЯсл и без них: данные РКП в исследовании J. Placzke и соавт. (Польша, 2023)1.
В реальной популяции пациентов, получавших лечение моноИТ, более длительная БРВ ассоциировалась с развитием НЯсл в период лечения. Разница в 2-летней БРВ в группах НЯсл+ и НЯсл- составила 20%1. При этом для комбоТТ более длительная БРВ не была связана с высокой частотой НЯсл1.
Учитывая, что спектр НЯ, развивающихся на фоне моноИТ, включает специфические иммуноопосредованные НЯ, которые часто переходят в хроническую форму (до 46%)8, 9 и/или требуют лечения глюкокортикостероидами (до 49%)10, 11, цена за не самое эффективное лечение (2-летняя БРВ в группе моноИТ на 10% ниже, чем в группе комбоТТ1) может показаться неоправданно высокой.
Авторы также отмечают, что развитие НЯсл 3 степени тяжести (по всей популяции пациентов) напротив было связано со значительным снижением ОВ1:
- 2-летняя ОВ в группе НЯсл+ 1 степени — 100%
- 2-летняя ОВ в группе НЯсл+ 2 степени — 93,8%
- 2-летняя ОВ в группе НЯсл+ 3 степени — 60,6%
Эти результаты вероятнее всего можно объяснить преждевременным прекращением терапии при развитии НЯсл 3 степени и связанным с этим снижением эффективности лечения1.
Предикторы выживаемости
Авторы исследования выделили ряд характеристик, связанных с худшим прогнозом ОВ и БРВ при проведении адъювантной терапии у пациентов с удаленной меланомой кожи1:
- Увеличение толщины первичной меланомы кожи (критерий T по классификации TNM) связано со снижением показателей ОВ и БРВ при проведении адъювантного лечения
- Изъязвление первичной меланомы кожи связано со снижением ОВ при проведении адъювантного лечения
Данные РКП также подтвердили, что завершающая лимфодиссекция после положительной БСЛУ не влияет на эффективность адъювантного лечения1.
Исследование РКП Bai X. и соавт. (международное исследование, 2023)
В исследовании Bai X. и соавт. были проанализированы данные 598 пациентов с меланомой кожи III стадии с мутацией BRAF V600. Из них 393 пациента получали адъювантную комбоТТ дабрафенибом и траметинибом, 205 пациентов – адъювантную моноИТ анти-PD-1 препаратами7.
На протяжении 3-летнего наблюдения показатели БРВ в группе комбоТТ были на 9,0—16,8% выше, чем в группе моноИТ (табл. 4)7. Показатели ОВ через 2, 3 и 4 года были близки в обеих группах (разница менее 5%), при этом 3-летняя ОВ была сопоставима с аналогичным показателем в исследовании COMBI-AD и составила 86%5, 7.
Таблица 4. Эффективность адъювантных комбоТТ и моноИТ после резекции меланомы кожи III стадии: данные Bai X. и соавт.7
Авторы исследования оценили эффективность моноИТ и комбоТТ в подгруппах пациентов в зависимости от пола, возраста, расы, характеристик исходной опухоли, а также проведения биопсии сторожевых лимфатических узлов и полной лимфодиссекции. Преимущество комбоТТ сохранялось во всех проанализированных подгруппах (табл. 5)7.
Таблица 5. Результаты подгруппового анализа комбоТТ и моноИТ в исследовании Bai X. и соавт.7
Что касается профилей безопасности комбоТТ и моноИТ в исследовании, важно отметить, что НЯ, развившиеся на фоне моноИТ, часто сохранялись в течение продолжительного времени после прекращения лечения. Так, у 14% пациентов более 3 месяцев после окончания моноИТ сохранялись эндокринные нарушения, у 5% — поражения кожи, у 3% — нарушения работы опорно-двигательного аппарата7.
Исследование РКП M. Haist и соавт. (Германия, 2023)
Результаты исследования Haist M. и соавт. подтверждают преимущество адъювантной комбоТТ по сравнению с моноИТ у пациентов с удаленной меланомой кожи в реальной клинической практике. Авторы проанализировали данные 515 пациентов, которым была выполнена адъювантная терапия после удаления меланомы кожи (табл. 6). 273 пациента получали моноИТ (ниволумаб или пембролизумаб), 242 пациента — комбоТТ (дабрафениб + траметиниб, Д+Т)2.
Таблица 6. Эффективность адъювантной комбоТТ и моноИТ после резекции меланомы кожи: данные РКП в исследовании Haist M. и соавт. (Германия, 2023)2.
При медиане наблюдения 21 месяц рецидив меланомы развился у 54,6% пациентов, получавших анти-PD-1, и только у 36,4% пациентов, получавших комбинацию Д+Т. Отдаленные метастазы также чаще диагностировали в группе моноИТ: 39,6% против 29,3% в группе комбинации Д+Т2. Медиана БРВ в группе Д+Т была почти в два раза больше, чем в группе моноИТ2.
Следует отметить, что у пациентов, получавших Д+Т, рецидивы чаще развивались после лечения, а на период проведения адъювантной терапии приходилось только 31,8% от всех рецидивов, в то время как у пациентов, получавших моноИТ, рецидив чаще развивался еще до окончания адъювантной терапии (63,1% от всех рецидивов)2.
Авторы исследования также провели интересный сравнительный анализ эффективности второй адъювантной ТТ и ИТ после повторной резекции меланомы кожи в связи с развитием локорегионарного рецидива или появлением метастазов в реальных условиях. У пациентов, получавших по поводу локорегионарного рецидива вторую адъювантную терапию комбинацией Д+Т, медиана БРВ была существенно длиннее, чем у пациентов, получавших моноИТ: 41 месяц против 6 месяцев2. При проведении второй адъювантной терапии у пациентов после удаления резектабельной меланомы кожи IV стадии медиана БРВ также была выше при применении Д+Т: 11 месяцев против 9 месяцев для моноИТ2.
Ключевые выводы
Изучив данные трех исследований РКП, ответим на поставленные в начале статьи вопросы.
Как соотносятся данные РКИ и РКП?
Эффективность комбоТТ в РКП на расширенной популяции пациентов (включая редкие мутации BRAF, увеличенный интервал до начала терапии, отсутствие лимфодиссекции) соответствовала или была выше, чем в РКИ1, 5, 7
- 2-летняя БРВ 66—75% в РКП против 67% в РКИ
- 2-летняя ОВ 88—91% в РКП против 91% в РКИ
Эффективность моноИТ анти-PD-1 по показателю 2-летней БРВ в реальных условиях соответствовала или была ниже, чем в РКИ1, 4, 6
- 2-летняя БРВ 56—64% в РКП против 62—68% в РКИ
Сохраняется ли преимущество комбоТТ перед моноИТ в реальных условиях?
Во всех рассмотренных исследованиях РКП, как и при проведении РКИ, адъювантная терапия комбинацией дабрафениб + траметиниб после удаления меланомы кожи показала более высокую эффективность, чем моноИТ1, 2, 7
- мБРВ на 6—14 месяцев дольше2, 7
- 2-летняя БРВ на 10—12% выше1, 7
Список сокращений
- БРВ — безрецидивная выживаемость;
- БСЛУ — биопсия сторожевых лимфатических узлов;
- Д+Т — комбинация дабрафениб + траметиниб;
- ИТ — иммуноонкологическая терапия;
- ВБОМ — выживаемость без отдаленных метастазов;
- комбоТТ — комбинированная таргетная терапия;
- мБРВ— медиана безрецидивной выживаемости;
- моноИТ — иммуноонкологическая терапия в монорежиме;
- НЯ — нежелательные явления;
- НЯсл — нежелательные явления, связанные с лечением;
- ОВ — общая выживаемость;
- РКИ — регистрационные клинические исследования;
- РКП — реальная клиническая практика;
- ТТ — таргетная терапия;
- НД — не достигнута.
Список литературы
- Placzke J. et al. Modern approach to melanoma adjuvant treatment with anti-PD1 immune check point inhibitors or BRAF/MEK targeted therapy: multicenter real-world report //Cancers. — 2023. — Т. 15. — № . 17. — С. 4384.
- Haist M. et al. Treatment management for BRAF-mutant melanoma patients with tumor recurrence on adjuvant therapy: a multicenter study from the prospective skin cancer registry ADOREG //Journal for Immunotherapy of Cancer. — 2023. — Т. 11. — № . 9.
- Новодережкина Е.А., Зырянов С.К. Роль данных реальной клинической практики в современном здравоохранении //Фармация. — 2021. — Т. 70. — № . 3. — С. 5–10.
- Eggermont A. M. M. et al. Adjuvant pembrolizumab versus placebo in resected stage III melanoma (EORTC 1325–MG/KEYNOTE-054): distant metastasis-free survival results from a double-blind, randomised, controlled, phase 3 trial //The lancet oncology. — 2021. — Т. 22. — № . 5. — С. 643–654.
- Long G. V. et al. Adjuvant dabrafenib plus trametinib in stage III BRAF-mutated melanoma //New England Journal of Medicine. — 2017. — Т. 377. — № . 19. — С. 1813–1823.
- Weber J. et al. Adjuvant nivolumab versus ipilimumab in resected stage III or IV melanoma //New England Journal of Medicine. — 2017. — Т. 377. — № . 19. — С. 1824–1835.
- Bai X. et al. Dabrafenib plus trametinib versus anti-PD–1 monotherapy as adjuvant therapy in BRAF V600-mutant stage III melanoma after definitive surgery: a multicenter, retrospective cohort study //EClinicalMedicine. — 2023. — Т. 65.
- Patrinely J. R. et al. Chronic immune-related adverse events following adjuvant anti-PD–1 therapy for high-risk resected melanoma //JAMA oncology. — 2021. — Т. 7. — № . 5. — С. 744–748.
- Goodman R. S. et al. Long-term outcomes of chronic immune-related adverse events from adjuvant anti-PD-1 therapy for high-risk resected melanoma. – 2023.
- O’Reilly A. et al. An immunotherapy survivor population: health-related quality of life and toxicity in patients with metastatic melanoma treated with immune checkpoint inhibitors //Supportive Care in Cancer. — 2020. — Т. 28. — С. 561–570.
- Mandala M. et al. Adjuvant nivolumab for stage III/IV melanoma: evaluation of safety outcomes and association with recurrence-free survival //Journal for immunotherapy of cancer. — 2021. — Т. 9. — № . 8.
11234830/ONCO/DIG/07.24/0