Введение
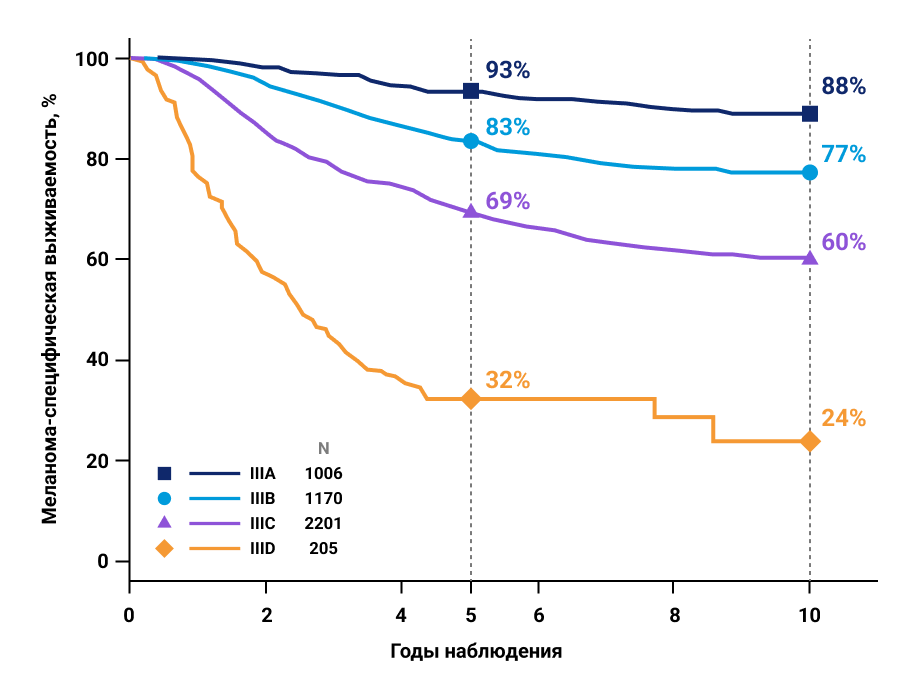
Пациенты с IIIА стадией представляют собой группу наиболее благоприятного прогноза среди всех пациентов с III стадией меланомы кожи. Так, 5-летняя меланома-специфическая выживаемость при IIIА стадии составляет 93% (против 83%, 69% и 32% у пациентов со стадиями IIIB, IIIC и IIID соответственно) (рис. 1)1.
Рисунок 1. Меланома-специфическая выживаемость у пациентов с меланомой кожи IIIA—D стадий1.
Согласно действующим клиническим рекомендациям пациентам после хирургического удаления меланомы кожи III стадии, в том числе IIIA подстадии, показано проведение адъювантной таргетной терапии (ТТ) комбинацией дабрафениб + траметиниб или иммуноонкологической терапии (ИТ) пембролизумабом2.
Возникает вопрос:
Если прогноз такой хороший, то зачем дополнительно назначать 12-месячный курс адъювантной лекарственной терапии?
Чтобы ответить на него, можно изучить данные соответствующих исследований. Однако в регистрационных клинических исследованиях3, 4 и в исследованиях реальной клинической практики7 данные по эффективности адъювантной терапии у пациентов с IIIА стадией меланомы кожи по классификаци AJCC 8 весьма ограничены в связи с небольшим количеством таких пациентов: COMBI-AD — 50 пациентов3, Keynote-054 — 42 пациента4, исследование реальной клинической практики Bai X. — 86 пациентов5. Имеются ли данные, полученные на большем количестве пациентов?
ASCO 2023: адъювантная таргетная терапия у пациентов с меланомой кожи IIIА стадии
На ASCO 2023 были представлены результаты многоцентрового ретроспективного клинического исследования эффективности адъювантной терапии после резекции меланомы кожи IIIА стадии (AJCC 8). В исследование были включены 628 пациентов из 34 исследовательских центров в Австралии, Европе и США. Медиана наблюдения составила 2,6 года6.
В исследовании были проанализированы результаты лечения в трех группах пациентов6:
- получавших ТТ комбинацией дабрафениб + траметиниб (n=80, все с мутацией BRAF)
- получавших адъювантную ИТ пембролизумабом или ниволумабом (n=256, из них с мутацией BRAF n=87)
- не получавших адъювантную терапию (n=292, из них с мутацией BRAF n=97)
Группы были сопоставимы по основным характеристикам (максимальный диаметр наибольшего метастатического очага в лимфатическом узле, доля пациентов N1a/N1b, число обнаруженных метастазов в лимфатических узлах, толщина меланомы по Бреслоу, митотический индекс)6.
В какой группе прогноз оказался лучше?
Пациенты, получавшие адъювантную ТТ, имели преимущество перед пациентами, получавшими ИТ или не получавшими лекарственное лечение, по всем показателям (1- и 2-летняя безрецидивная выживаемость (БРВ), 1- и 2-летняя выживаемость без отдаленных метастазов (ВБОМ)6. Наиболее значительная разница была получена по показателю 2-летней БРВ: в группе ТТ она оказалась на 27% выше, чем в группе ИТ (98,5% против 71,6%)6.
Таблица 1. Основные результаты исследования эффективности адъювантной терапии после резекции BRAF+ меланомы IIIА стадии (P. Grover и соавт.)6.
Что касается безопасности адъювантной терапии, как было показано в более ранних исследованиях5, 7, 8, 9, НЯ при ИТ часто переходили в хроническую форму: частота неразрешенных НЯ при последнем наблюдении составила 26,9% в группе ИТ6.
Выводы
- Согласно современным клиническим рекомендациям после удаления меланомы кожи IIIА стадии (AJCC 8) пациентам показано проведение адъювантной терапии, несмотря на благоприятный прогноз2.
- Прогноз после адъювантной ТТ лучше, чем после адъювантной ИТ: 2-летняя БРВ 98,5% против 71,6% в группе ИТ и 83,4% в группе без лечения6.
- Каждый четвертый пациент, получивший адъювантную ИТ, сталкивается с хроническими НЯ, которые существенно снижают качество жизни6.
Список сокращений
- ВБОМ — выживаемость без отдаленных метастазов;
- БРВ — безрецидивная выживаемость;
- ИТ — иммуноонкологическая терапия;
- НЯ — нежелательные явления;
- ТТ — таргетная терапия.
Список литературы
- Keung E. Z., Gershenwald J. E. The eighth edition American Joint Committee on Cancer (AJCC) melanomastaging system: implications for melanoma treatment and care // Expert review of anticancer therapy. — 2018. — Vol. 18. — № 8. — P. 775–784.
- Клинические рекомендации Министерства здравоохранения РФ «Меланома кожи и слизистых оболочек (взрослые)») // Рубрикатор клинических рекомендаций. URL: https://cr.minzdrav.gov.ru/schema/546_3 (дата обращения: 16 июня 2024 г.).
- Dummer R. et al. Five-year analysis of adjuvant dabrafenib plus trametinib in stage III melanoma //New England Journal of Medicine. — 2020. — Т. 383. — № . 12. — С. 1139–1148.
- Eggermont A. M. M. et al. Five-year analysis of adjuvant pembrolizumab or placebo in stage III melanoma //NEJM evidence. — 2022. — Т. 1. — № . 11. — С. EVIDoa2200214.
- Tong J. et al. Long-term toxicities of immune checkpoint inhibitor (ICI) in melanoma patients // Current Oncology. — 2022. — Т. 29. — № . 10. — С. 7953–7963.
- Grover P. et al. Efficacy of adjuvant therapy in patients (pts) with AJCC v8 stage IIIA cutaneous melanoma // ASCO Annual Meeting. — 2023. https://meetings.asco.org/abstracts-presentations/218508.
- Eggermont A. M. M. et al. Adjuvant pembrolizumab versus placebo in resected stage III melanoma (EORTC 1325–MG/KEYNOTE-054): distant metastasis-free survival results from a double-blind, randomised, controlled, phase 3 trial //The lancet oncology. — 2021. — Т. 22. — № . 5. — С. 643–654.
- Long G. V. et al. Adjuvant dabrafenib plus trametinib in stage III BRAF-mutated melanoma //New England Journal of Medicine. — 2017. — Т. 377. — № . 19. — С. 1813–1823.
- Patrinely J. R. et al. Chronic immune-related adverse events following adjuvant anti-PD–1 therapy for high-risk resected melanoma // JAMA oncology. — 2021. — Т. 7. — № . 5. — С. 744–748.
11244858/ONCO/DIG/08.24/0